查疾病
您的当前位置:首页 > 查疾病 > 恶性组织细胞病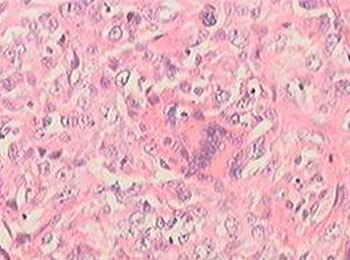
恶性组织细胞病(恶组)是单核—巨噬细胞系统中组织细胞的恶性增生性疾病。临床表现以发热、肝脾淋巴结肿大、全血细胞减少和进行性衰竭为特征。恶组多见于青壮年,以20~40岁者居多,男女发病为2~3:1。本病按病程可分为急性和慢性型。国内以急性型为多见。起病…
查看详细早期症状:发热为其首见及常见症状,多为不规则高热。
晚期症状:全血细胞减少引起的贫血、感染、出血。肝、脾和淋巴结肿大,肺部病变多见,咳嗽、咳血甚至呼吸衰竭
相关症状:便血 衰老加快 斑丘疹 鼻衄
一、症状
根据恶组细胞浸润部位的不同,临床上可有不同的表现,从上述病理累及部位来看可累及造血组织(最常见),又可累及非造血组织,因此临床表现多种多样。国内作者曾提出不少分型意见,如按Israels分为5型,实则多数恶组病理、临床表现具有2型以上的特点。虽然Cazal将其简化为内脏型、皮肤型、儿童型,但认为儿童与成人临床差异不大。有提出病变主要累及造血组织称普通型,主要累及非造血组织则称特殊型。有关特殊型提法更多,如,皮肤型、胃肠型、肺型、肾型、神经型、多发性浆膜炎型、肠穿孔型、巨脾及脾自发破裂型、慢性复发型,等等。也有作者认为临床表现多样,难以某型概括,临床与病理对照也不尽一致,认为分型对预后意义不大。对待分型国内目前尚无统一意见。此外,有提出根据病程分急性和慢性(1年以上为慢性),由于慢性很少见,大多数病例发病急、病程短,故临床上未强调急、慢之分。1975年在福建三明市召开的恶组座谈会上对慢性型未作定论。现将国内文献报道(包括特殊类型)的862例综合分析如下,以了解临床表现的多样性。
1、首发症状:不论是何种类型的恶组,发热常是首发表现。热型以不规则高热居多(38.7%)、其次为稽留热(26.3%)、弛张热(21.2%),间歇热(10.8%)及低热(3%)少见。苍白、乏力是因贫血所致,出血倾向在首发表现中亦不少见,尤其到病程晚期愈来愈重是致死原因之一。黄疸一般在早期常不明显多在较晚期出现,但也有部分患者以黄疸首发而住入传染病医院。此外,国内报道不少例以发热、腹痛及反复血便首发,因常伴有肠穿孔而误为急腹症入外科手术探查。再有恶组侵犯肺部而误为肺炎、肺部肿瘤、肺结核的报道亦不断涌现。另有以截瘫、脑神经麻痹或颅内压增高为首发表现者有不少个案报道。值得提出的有的患者骨、关节痛常很显著,止痛药物常无效。
2、体征:肝大、脾大是常见的体征,常呈轻度或中度肿大,1例肝最大在右肋下10cm;1例脾最大入盆腔。但在胃肠型恶组约1/3病例肝、脾未触及,2/3肿大者为轻度肿大。表浅淋巴结一般似黄豆大、花生米大、最大如鸡蛋大。从尸检情况看,恶组主要侵犯深部淋巴结,浅表淋巴结不大并不能排除恶组。皮肤损害以结节和肿块最为常见(可形成肉芽肿或导致纤维化,肉眼上形成结节,但镜下细胞彼此并不黏聚),并可伴有溃疡,尚可伴有非特异性损害,如斑丘疹、紫癜及红皮病等。皮肤损害在儿童恶组中较为多见,并被认为是其特征。肺部可有啰音伴有咳嗽、气短。腹部触及肿块者多为肠型恶组之体征,有人统计53例以肠道症状首发者(除发热、腹痛、腹泻外),腹部触及肿块占41.5%,而发生肠穿孔者高达52.8%。
二、诊断
过去诊断本病主要仍依靠临床表现和细胞形态学或活体组织病理检查结果,近年来对本病的恶性细胞来源有了新的认识,甚至提出应当更改病名,但作为同一个疾病实体,它的临床表现和细胞、病理形态所见与过去的描述不应有差别,因而过去的诊断依据仍沿用,只是需要增加一些细胞标志、细胞和分子遗传学方面的指标以确定恶性细胞的来源,以便准确地对疾病命名。
1、临床表现:以发病急、长期发热,伴进行性肝脾淋巴结肿大、进行性肝肾功能衰竭、进行性全血细胞减少、进行性全身衰竭为特点,常伴黄疸、出血,可有皮肤损害和浆膜腔积液。
2、骨髓涂片:确诊必须找到一定数量的上述的异常细胞。由于骨髓不一定经常受累,且病变常呈灶性分布,因此骨髓1~2次检查阴性不能除外本病,需多次重复检查。国内有人提出胸骨穿刺阳性率高于髂骨(4例髂骨阴性改作胸骨穿刺均呈阳性,又有数例髂骨穿刺涂片异常细胞只占1%,换作胸骨穿刺则异常细胞占有核细胞的8%)。
3、外周血浓缩涂片检查:统计305例外周血涂片有152例(49.8%)找到异常细胞。血液浓集后找到异常细胞的机会更高些。血液浓缩涂片可与骨髓涂片相互补充参照。
目前主要诊断恶组的方法是依靠骨髓穿刺涂片检查。骨髓1次确诊的成功率为69%,骨髓找到“恶组”细胞占有核细胞的2%~78%(其中占2%~20%为77.1%,占72%以上为22.9%)。有人提出通过5次的骨髓穿刺,98%的病例可以诊断。实际上生前未能确诊的仍有10.2%患者,而另有10.3%患者需依靠其他部位的活组织采取病理检查。关于其他部位活组织采取确诊的成功率:皮肤活检72.7%(24/33);淋巴结活检63.1%(70/111);骨髓活检39.7%(27/68);肝脏活检25%(5/25),此外有个别作淋巴结穿刺,脾穿刺,心包穿刺,肺穿刺,脑脊液及胸腹水找到“恶组”细胞。浅表淋巴结活检成功率低于皮肤活检是由于“恶组”多侵犯深部淋巴结,而骨髓活检及肝活检只能做辅助诊断是由于“恶组”常呈灶性浸润,穿刺不易抓到。
总之,关于诊断必须强调临床表现的重要性,国内不少学者同意作者(1973)的观点,即临床怀疑本病又有形态学支持则可初步诊断;临床怀疑而无形态学变化不能排除本病,应反复进行多部位骨髓穿刺(胸骨穿刺阳性率可能较高)及可能的活组织病理检查;有形态学特点但与临床表现不符者,需与反应性及其他组织细胞增生性疾病相鉴别。为确定恶性细胞来源,应作多种细胞化学、免疫标志以及细胞和分子遗传学检查,Ki-30(CD30)阳性,t(2:5)(p23:q35)染色体移位,有融合基因NPM/ALK(p80)者,有助于确定为间变性大细胞淋巴瘤,其他标记物如上皮膜抗原(epithelial membrane antigen, EMA)和CD25(IL-2受体)也可能阳性。
一、发病原因
目前尚不清楚,通常认为是组织细胞性淋巴瘤或急性单核细胞性白血病的一种变型,可能与EB 病毒感染有关,亦有人士认为是自身免疫增殖性疾病或者由于免疫功能缺陷所致。近年来报道恶组常作为继发于其他肿瘤的第2个恶性肿瘤,常伴发于恶性淋巴瘤(B 细胞性)、T 细胞性和裸细胞性急性淋巴细胞性白血病、急性粒—单核细胞白血病、 Lennerts 淋巴瘤。推测可能于化疗或原发肿瘤抑制免疫系统,导致染色体异常,克隆恶性突变有关。本病的发生可能与患者的免疫功能低下有关。由于尸检中部分病例有肥大细胞增生现象有人认为是一种自身免疫增殖性病变,初为过敏,渐转化为肿瘤。有人注意到恶组患者血清EB病毒抗体效价增高,怀疑本病与病毒感染有关。已知EB病毒是引起Burkitt淋巴瘤的病因,但在恶组病因中起何作用尚不清楚。有人注意到近年来恶组在中非地区发病率有所上升,推测可能与环境因素特别是与病毒因素有关。但目前尚缺乏有力的血清学和流行病学证据。Kobari等观察到1例慢性EBV感染病人后发生恶组,通过PCR法扩增,EBV定位于淋巴细胞膜的抗原,用原位杂交法(ISH)检测DNA中的EBV,结果发现早期慢性感染时非恶性的组织细胞中存在的EBV颗粒与后来的恶组细胞中的EBV颗粒相同。由此推论可能原本正常的组织细胞受EBV感染后变成异常细胞,并发生克隆性扩增,结果产生恶组。国内梁平(1984)对8例恶组骨髓标本做电镜观察,在2例恶组细胞内见到Ⅳ型核小体,认为它是细胞曾受病毒作用的一个形态学标志。国外有人怀疑本病与遗传因素有关,有父子先后发病的报道。国内关敏等(1990)报道有2例为同胞兄弟,且其家系中另有1兄弟患病,3兄弟均在婴幼儿时期发病,病情相同且均在发病后3个月内死亡。近年来国内学者发现恶组尸检中全身淋巴组织呈现重度萎缩,推测患者伴有免疫功能缺陷。至于免疫缺陷是病因还是结果尚无定论。总之,病因至今仍不明确。
二、发病机制
目前不明。1969年Rodman报道了2例恶组有染色体易位,即t(2;5)(p23;q35),此外尚有1号染色体异常。Morgan等在1986年发现恶组细胞株中5号染色体长臂一固定点的断裂(5q35断裂),并常伴有t(2;5)。另有报道1号、3号和6号染色体也有易位。Morris(1994)等证实t(2;5)可产生NPM/ALK融合基因。Shiota等(1995)指出,此融合基因编码一个(80kD)的高磷酸化蛋白(p80),NPM/ALK融合基因和p80见于所有t(2;5)的病例中,但能表达p80 NPM/ALK者是一个独立的病种。通过细胞遗传学或p80表达的测定,5q35断裂目前可作为诊断CD30阳性肿瘤的前提。国内吴士琪等(1983)提出D组染色体丢失1条是本病较常见的核型。1989年Stephen等报道了3例“恶组”,均表达ki-1(CD30),皆有t(2;5)(p23;q35)易位,认为这种易位可能是具有恶组特点的一组病共有的特征。1990年Abe等研究了4例恶组的细胞遗传学,其中2例有17号染色体异常,断点在短臂13(17p13)。复习文献另有7例恶组亦有相同异常发现。现已有证明p53基因突变在人类恶性肿瘤的发生率较高,而p53(抑癌基因)即定位于17号染色体短臂。1992年国内田虹等对2例恶组白血病型患者进行骨髓染色体分析,均出现1号部分三体(1qter-1p11)和1p11断裂易位。
常见并发症:贫血 消化道出血
本病的并发症有高热衰竭、出血和感染,严重者可导致死亡。恶组病变常累及多个脏器,尤其是急性型,起病急,病程短暂且凶险,可出现发热、贫血、出血、肝、脾、淋巴结肿大,咳嗽、胸痛、呼吸困难、腹痛、消化道出血等。这些即是它的临床表现,同是亦是它的并发症,在临床上很难加以区别。



