发布时间:2020年04月15日 14:43:50 来源:振东健康网
一、概述
肾细胞癌(renal cell carcinoma,RCC,简称肾癌)是起源于肾小管上皮的恶性肿瘤,占肾脏恶性肿瘤的80%~90%。肾癌的组织病理类型最常见的为透明细胞癌,其次为乳头状肾细胞癌及嫌色细胞癌,以及集合管癌等少见类型的肾细胞癌。肾癌发病率仅次于前列腺癌及膀胱癌,占泌尿系统肿瘤第三位。
随着医学影像学的发展,早期肾癌的发现率逐渐增长,局限性肾癌经过根治性肾切除术或者保留肾单位的肾脏肿瘤切除术可获得满意的疗效。据统计,目前确诊时既已属晚期的患者已由数年前的30%下降至17%,随着靶向治疗的持续发展及新型免疫治疗药物的兴起,晚期肾癌的疗效也逐步得到改善。
二、流行病学及病因学
(一)流行病学
在世界范围内,肾癌的发病率约占成人恶性肿瘤的3%,其分布具有明显的地域差异,北美、西欧等西方发达国家发病率最高,而非洲及亚洲等发展中国家发病率最低。全世界范围内,肾癌发病目前排在男性恶性肿瘤第9位(21.4万例新患者)及女性第14位(12.4万例新患者),其男女发病率约为2∶1,发病高峰在60~70岁。根据GLOBOCAN 2012年世界恶性肿瘤流行病学研究数据,肾癌的全球发病率居恶性肿瘤第14位,死亡率居第16位。近几十年来,在大多数国家和地区肾癌的发病率都呈现持续增长趋势,包括北美、部分欧洲、亚洲、大洋洲及部分拉丁美洲,但肾癌的死亡率在发达国家中趋于稳定或下降。据中国肿瘤登记年报的资料显示,从1988年至2014年我国肾癌的发病率为上升趋势。人口结构老龄化、生活方式西方化及早期筛查的推广可能是发病率增高的原因。2005年至2009年肾癌的发病率分别为3.96/10万、4.44/10万、4.64/10万、5.08/10万、4.5/10万。2018年2月,国家癌症中心发布了最新癌症数据,汇总了339家癌症登记点的数据,共覆盖中国2.8亿人群。数据显示,2014年中国肾癌发病率为4.99/10万,其中男性肾癌发病率为6.09/10万,女性肾癌发病率为3.84/10万。
(二)病因学
肾癌的病因尚不明确,其发病与遗传、吸烟、肥胖、高血压及抗高血压药物等有关。吸烟和肥胖是最公认的致肾癌危险因素。
⒈遗传性因素:大部分肾细胞癌是散发性的,遗传性肾癌占肾癌总数的2%~4%,多以常染色体显性遗传方式在家族中遗传,由不同的遗传基因变异造成,这些基因既包括抑癌基因又包括癌基因。已明确的遗传性肾癌包括VHL(von Hippel–Lindau)综合征(双侧多发的肾透明细胞癌和肾囊肿)、MET基因相关的遗传性乳头状肾细胞癌(Ⅰ型)、延胡索酸水化酶基因异常引起的遗传性平滑肌瘤病和肾细胞癌(非Ⅰ型乳头状肾细胞癌)、BHD(Birt-Hogg-Dube)综合征(多发性肾嫌色细胞癌、杂合性嫌色细胞和嗜酸细胞肾肿瘤、乳头状肾细胞癌)、HRPT2基因相关的甲状旁腺功能亢进-颌骨肿瘤综合征(混合型上皮和基质肿瘤、乳头状肾细胞癌)(表1)。一般认为如下人群可能是遗传性肾癌的潜在患者:①≤45岁的肾癌患者;②双侧/多发肾脏肿瘤;③肾癌家族史(至少1个一级亲属,至少2个二级亲属);④肾癌合并其他肿瘤病史(嗜铬细胞瘤,胃肠道间质瘤,神经系统血管母细胞瘤,胰腺神经内分泌肿瘤等),合并其他病变如肺囊肿,自发性气胸等;⑤合并少见的皮肤病变(平滑肌肉瘤,血管纤维瘤等);⑥个人或家族有肾癌相关综合征病史。对于这部分患者,可以建议本人及相关家属进行基因突变检测。

2.吸烟:吸烟是肾癌发病因素之一。大量的前瞻性研究观察了肾癌与吸烟的关系,认为吸烟是中等度危险因素。既往曾有吸烟史的人患肾癌的相对危险度为1.3;而正在吸烟的人患肾癌的相对危险度为1.6。吸烟是目前唯一公认的肾癌环境危险因素。
3.肥胖:肥胖程度一般用体重指数(body mass index,BMI)来表示,体重指数指数增加,则患肾癌的危险性增加。肥胖增加肾癌风险的具体机制还未明,可能和肥胖增加雄性激素及雌性激素释放,或者与脂肪细胞释放的一些细胞因子相关。
4.高血压及抗高血压药物:一些大型研究显示高血压和其相关药物使用可能是肾癌发病因素之一。高血压病患者、使用利尿剂特别是噻嗪类利尿药以及其他抗高血压药物的人,患肾癌的危险性会增加1.4~2倍。很难区分到底是高血压本身还是抗高血压药物引起肾癌,因为在所有研究中这两者往往都是同时存在的。但是若能更好地控制血压,那么肾癌的发病风险会下降,因此抗高血压药物可能不是发病风险之一。
5.与终末期肾病长期透析相关的获得性囊性肾脏疾病(ARCD):与普通人相比有终末期肾病患者的肾癌发病率更高。长期透析的患者容易患获得性肾囊肿性疾病,这可能是由于肾组织内的细胞无序增殖的结果。这类患者的肾癌和传统肾癌有一定区别:发病年龄更年轻,而且男女比更高。在这些肾癌患者中,肿瘤通常是双侧、多发的,组织病理学上呈现乳头状结构。因此,对终末期肾病患者应该定期进行B超或增强MRI检查。对于透析患者,即使肾癌小于4cm,也首选根治性肾切除术。
6.其他:有证据表明,饮酒、职业暴露于三氯乙烯、石棉、多环芳香烃等物质,以及高雌激素的女性等都有可能增加患肾癌的风险。总的来说,目前无法找到一种与肾癌具有明确关系的致癌物质,尚需要进一步研究遗传因素与环境暴露之间相互作用的潜在影响。
三、组织病理学
(一)大体病理
绝大多数肾癌发生于一侧肾脏,双侧肾癌(异时或同时)仅占散发性肾癌的2%~4%。肾肿瘤常为单发肿瘤,其中10%~20%为多发病灶。多发病灶病例常见于遗传性肾癌以及乳头状肾癌的患者。肿瘤瘤体大小差异较大,常有假包膜与周围肾组织相隔。
(二)分类
1981年、1997年、2004年及2016年WHO共推出过4个版本的肾脏肿瘤分类标准。目前临床上使用的是2016年WHO第四版肾脏肿瘤分类标准(表2),其沿用了2004年版本的框架,仅对一些认识有深入的肿瘤进行了分类命名上的调整:如将未见有复发转移报导的多房囊性肾细胞癌更新为多房囊性肾细胞肿瘤,再如将Xp11.2易位/TFE3融合基因相关性肾癌归入MiT家族转位性癌,后者还包括TFEB基因转位的肾细胞癌等。此外,也新增了部分新的病理亚型。如前所述,肾癌依据与遗传综合征关系可分成遗传性肾癌和散发性肾癌。单纯从病理形态不能区分遗传性肾癌和散发性肾癌。

1.常见肾细胞癌病理类型特征
⑴透明细胞癌
透明细胞癌(clear cell renal cell carcinoma,ccRCC)是最常见的肾癌病理亚型,约占肾癌的60%~85%。既往曾使用的肾颗粒细胞癌因为在其他类型的肾癌亚型中也能见到胞质嗜酸性的颗粒细胞,胞质中的颗粒不再是肾颗粒细胞癌的专有特征,不在列为单独病理类型。因肾颗粒细胞癌细胞核分级的级别高,现将其归为高分级的ccRCC。
1)大体检查:双侧肾脏发病率相等,少于5%的病例可呈多中心性发生或累及双侧肾脏。表现为肾皮质内实性球形结节,与周围肾组织界限清楚或不清,可见假包膜;因癌细胞中含有丰富的脂质,切面呈金黄色。肿瘤中常见出血、坏死、囊性变,而呈现多彩状外观,偶见钙化或骨化。
2)组织病理学:癌细胞胞质透明或嗜酸性,胞膜清楚;组织中可见小的薄壁血管构成的网状间隔;肿瘤细胞呈巢状和腺泡状结构;呈肉瘤样分化的肿瘤区域中可见到瘤巨细胞,呈横纺肌分化的肿瘤细胞可见到宽的嗜酸性胞质伴有偏位细胞核,可见突出核仁,提示预后不良;部分肿瘤中可见坏死、纤维黏液样间质及钙化、骨化。
3)常用的免疫组化抗体:CK8、CK18、vimentin、CA IX、CD10和EMA阳性。
⑵乳头状肾细胞癌
乳头状肾细胞癌(papillary renal cell carcinoma,PRCC)约占肾癌的7%~14%。国内有些专业书籍将其翻译成嗜色细胞癌。其发病年龄、性别、男女发病率比例、症状和体征与肾透明细胞癌相似。就诊时大多数病例处于Ⅰ期。
1)大体检查:病变累及双侧肾脏和多灶性者较透明细胞癌多见;大体多呈灰粉色,出血、坏死、囊性变多见。
2)组织病理学:根据组织病理学改变将其分为Ⅰ型和Ⅱ型两个亚型。肿瘤细胞呈乳头状或小管状结构,乳头核心可见泡沫状巨噬细胞和胆固醇结晶;肿瘤细胞较小,胞质稀少(Ⅰ型)或肿瘤细胞胞质丰富嗜酸性,瘤细胞核分级高(Ⅱ型),可见坏死、肉瘤样分化及横纹肌样分化区域。研究显示,Ⅰ型PRCC患者生存期明显优于Ⅱ型患者。
3)常用的免疫组化抗体:与ccRCC相似,现有的研究认为,乳头状肾细胞癌CK7呈阳性,P504S阳性率较高,且Ⅰ型较Ⅱ型阳性率为高。
⑶嫌色细胞癌
嫌色细胞癌(chromophobe renal cell carcinoma,CRCC)约占肾癌的4%~10%。平均发病年龄60岁,男女发病率大致相等。与其他肾癌亚型相比无特殊的临床症状和体征。影像学上特征多显示瘤体较大,肿瘤密度或信号均匀,无出血、坏死和钙化。
1)大体检查:肿瘤无包膜但边界清楚,大小4~20cm,切面呈质地均一的褐色,可见有坏死,但出血灶少见。
2)组织病理学:肿瘤呈实体性结构,可出现灶状钙化及厚纤维间隔;与透明细胞癌不同,瘤体中的血管为厚壁血管,而非薄壁血管;瘤细胞体积大,呈多角形,胞质透明略呈网状,细胞膜非常清晰(嫌色细胞),亦可见嗜酸性胞质的瘤细胞,瘤细胞核的核周空晕是此型的特征之一,并可见双核细胞;Hale胶体铁染色示肿瘤细胞质呈弥漫阳性。近年来研究发现嫌色细胞癌存在嗜酸细胞型亚型,其组织学特征包括:小细胞伴有纤细的嗜酸性颗粒状胞质;嗜酸性细胞位于细胞巢的中央,而胞质苍白的细胞位于细胞巢的周边处;细胞核不规则皱缩,染色质凝聚呈块状,可见双核细胞和核周空晕;也可见圆形的细胞
3)常用的免疫组化抗体:CK7阳性,CD117阳性,vimentin阴性,CMA弥漫阳性,lectins和parvalbumin阳性,肾细胞癌抗原弱阳性,CD10阴性。
4)特殊染色:胞质呈Hale胶体铁阳性反应。
⑷低度恶性潜能多房囊性肾细胞性肿瘤
在2016年之前的版本,这一肿瘤被称为多房囊性肾细胞癌。肿瘤由无数的囊肿组成,囊壁含单个或簇状透明细胞,无膨胀性生长;形态与透明细胞癌(G1/2)不能区分,无坏死、脉管侵犯及肉瘤样分化。需与肾透明细胞癌囊性变、广泛玻璃样变、出血以及含铁血黄素沉着相鉴别。免疫表型与ccRCC相似。
⑸集合管癌和肾髓质癌
Bellini集合管癌(carcinoma of the collecting ducts of Bellini)是指来源于Bellini集合管的恶性上皮性肿瘤;肾髓质癌(renal medullary carcinoma)来源于近皮质区的集合管,患者几乎均伴有镰状细胞性血液病。两者从大体及组织学表现有一定相似性,一并介绍。
1)大体检查:两者均发生于肾中央部分,切面实性,灰白色,边界不清,可见坏死。
2)组织病理学:需要指出的是,Bellini集合管癌常为排除性诊断,肿瘤部位对于作出诊断很重要,组织学上可见不规则的小管状结构,细胞高度异型性;肾髓质癌镜下呈低分化的、片状分布的肿瘤,瘤细胞排列呈腺样囊性结构,瘤体内可见较多的中性粒细胞浸润,同时可见镰状红细胞。
3)常用的免疫组化抗体:两者常见的免疫组化组合包括PAX2、PAX8、OCT3/4、SMARCB1/INI1、P63。
2.少见肾细胞癌病理类型特征
(1)MiT家族转位癌
包括两类肿瘤,分别与两个转录因子(TFE3和TFEB)出现融合基因相关。Xp11转位造成TFE3基因的融合;t(6;11)造成MALAT1-TFEB融合。这一肿瘤在儿童期多见,仅占成人期RCC中的1.6%∼4%。t(6;11)RCC较Xp11转位RCC少见。大体不具有特征性。镜下,Xp11转位性肾细胞癌表现为由透明细胞形成的乳头,伴有散在砂粒体沉着;而t(6;11)转位性肾细胞癌表现为大小细胞组成的细胞巢,其内可见基底膜样物质沉着。免疫组化表现为:上皮标记物表达下降,如CK、EMA;表达PAX8及其他肾小管标记物;t(6;11)RCC恒定表达黑色素标记物,如HMB45、Melan A 以及Cathepsin K、TFEB;而Xp11 RCC:部分表达黑色素标记物及TFE3。
(2)获得性囊性肾疾病相关性肾细胞癌
此类肿瘤常见于终末期肾病以及有获得性肾囊肿病的病史,最常伴发于长期进行血液透析的患者。大体常为双侧性、多灶性病变,边界清楚,周围可见多囊肾背景。组织学表现为以微囊结构、丰富的肿瘤内嗜酸性草酸盐结晶沉积特征。免疫组化表现为RCC、CD10及AMACR阳性,CK7阴性。
(3)透明细胞乳头状肾细胞癌
此类肿瘤占肾肿瘤的1%∼4%,无性别倾向,呈散发或伴发于终末期肾病、VHL综合征。大体表现为体积较小,边界清楚有包膜的肿物,常可见囊性变。组织学表现为乳头状结构,细胞较一致,胞质透明,核远离基底膜排列,可见胞突,G1或G2细胞核分级,并未见肿瘤坏死、肾外侵犯、脉管瘤栓。免疫组化表现为:CK7弥漫阳性,CAIX呈杯口状状阳性,P504S阴性;PAX2、PAX8及CK34bE12阳性,CD10阴性。
(4)遗传性平滑肌瘤病和肾细胞癌相关性肾细胞癌
遗传性平滑肌瘤病和肾细胞癌相关性肾细胞癌是一类伴有FH基因胚系突变的肾细胞癌,伴发肾外平滑肌瘤病。大体肿瘤可呈囊性改变,伴有明显的附壁结节。
形态与乳头状肾细胞癌形态或与集合管癌形态有重合;细胞核可见核内包涵体,并可见核周空晕。免疫组化表现为延胡索酸水合酶(FH)表达缺失。
(5)琥珀酸脱氢酶缺陷型肾细胞癌
此类肿瘤罕见,多为遗传性肿瘤。大体多呈边界清楚实性肿物。肿瘤细胞排列呈实性,巢状或小管状结构;胞质空泡状嗜酸性至透明,核轮廓规则光滑,染色质细腻,核仁不明显(类似与神经内分泌细胞);胞质空泡状;偶见高级别细胞核。免疫组化呈SDHB表达缺失。
(6)管状囊性癌
此类肿瘤罕见,常为体检偶发肿瘤。大体呈灰白海绵样或瑞士奶酪样外观。镜下呈小到中等大小小管伴有大囊形成,单层扁平、立方或柱状上皮,可见鞋钉状细胞;相当于G3的细胞核。免疫组化表达高分子量角蛋白。
(7)黏液小管样梭形细胞癌
此类肿瘤不足肾脏肿瘤1%。大体呈边界清楚的实性肿物。组织学表现为拉长或相互吻合的小管状结构,部分区域可见梭形细胞;核呈低级别;间质呈嗜碱性黏液样。免疫组化呈CK7,PAX2以及P504S阳性。
(8)肾细胞癌,未分类
目前包括不具备现有肾细胞癌亚型特征的癌,可以低级别或高级别。包括以下类型:含有一种以上肾细胞癌的病理特征、伴有黏液分泌的肾细胞癌、伴有未分类上皮成分的肾细胞癌、低级别或高级别未分类的嗜酸性肿瘤以及肉瘤样癌等。随着对肾细胞癌认识的深入,这一分类所占比例将越来越小。
(三)分级
病理分级是一个重要的预后相关因素,只适用于透明细胞癌和乳头状肾细胞癌。在以往的WHO分类版本中,最为常用的是1982年Fuhrman四级分类。1997年WHO推荐将Fuhrman分级中的Ⅰ、Ⅱ级合并为一级即高分化、Ⅲ级为中分化、Ⅳ级为低分化或未分化。2016版病理分级在原Fuhrman四级分级系统上做了进一步调整,增加了客观评价标准,形成WHO/ISUP病理分级系统(表3),使之在实践中操作性更强,重复性更好。

(四)分期
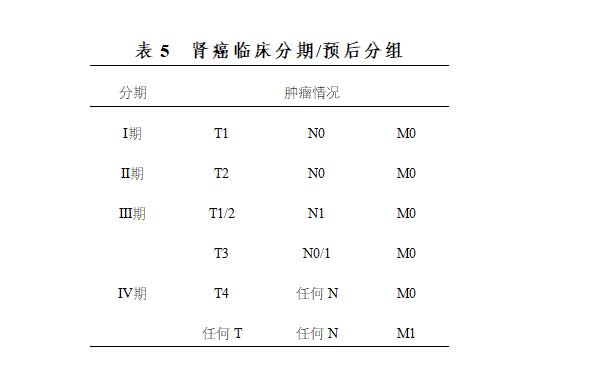
肾癌分期采用最广泛的是美国癌症分期联合委员会(American Joint Committee on Cancer Staging,AJCC)制定的TNM分期系统,目前应用的是2017年更新的第8版(表4、表5)。

四、诊断
(一)临床表现
肾癌患者的临床表现复杂、多变,这些临床表现有些是肾肿瘤本身直接导致的,有些可能是由于肾癌细胞所分泌的激素或转移灶所产生。由于健康体检越来越普及,来医院就诊的多数肾癌患者通常是由影像学检查无意中被发现。
在临床中,早期肾癌往往缺乏临床表现。当经典的肾癌三联征:血尿、腰痛和腹部包块都出现时,约60%的患者至少已达T3期;当出现左侧精索静脉曲张时,提示可能合并左肾静脉瘤栓。因此早期诊断RCC 具有重要意义。
副瘤综合征:临床表现不是由原发肿瘤或转移灶所在部位直接引起,而是由于肿瘤分泌的产物间接引起的异常免疫反应或其他不明原因引起的机体内分泌、神经、消化、造血、骨关节、肾脏及皮肤等系统发生病变,并出现相应的临床表现,被称为副瘤综合征。肾癌患者副瘤综合征发生率约30%,表现为高血压、红细胞沉降率增快、红细胞增多症、肝功能异常、高钙血症、高血糖、神经肌肉病变、淀粉样变性、溢乳症、凝血机制异常等。出现副瘤综合征的患者预后更差。
转移性灶引起的症状:部分肾癌患者是以转移灶的临床表现为首发症状就诊,如骨痛、骨折、咳嗽、咯血等。体格检查发现包括颈部淋巴结肿大、继发性精索静脉曲张及双下肢水肿等,后者提示肿瘤侵犯肾静脉和下腔静脉可能。在转移性肾癌患者中,常见的转移脏器及转移发生率依次为:肺转移(48.4%)、骨转移(23.2%)、肝转移(12.9%)、肾上腺转移(5.2%)、皮肤转移(1.9%)、脑转移(1.3%)、其他部位等(7.1%)。
(二)实验室检查
肾癌实验室常规检查的目的是了解患者的一般状况以及是否适于采取相应的治疗措施,主要包括尿常规、血常规、红细胞沉降率、血糖、血钙、肾功能(血尿素氮、血肌酐和肾小球滤过率)、肝功能、乳酸脱氢酶、碱性磷酸酶等项目。如需进行有创检查或手术治疗,则应进行必要的凝血功能检测。以上项目的检查结果在肾癌患者中通常会表现为血尿、红细胞增多及低血红蛋白、红细胞沉降率增快、高血糖、高血钙、肾功能异常及肝功能异常等。对邻近或累及肾盂的肾肿瘤患者还需做尿细胞学检查。对孤立肾的肾肿瘤、双肾肿瘤、肾功能指标异常和存在使肾功能受损的疾病(如糖尿病、慢性肾盂肾炎、多囊肾、对侧肾结石等)患者需行核素肾图检查,了解肾功能情况,并对肾功能不全等级进行评定。目前,尚无公认的用于肾癌早期辅助诊断的血清肿瘤标志物。
(三)影像学检查
随着影像学检查的普及,目前超过50%的肾癌是在对腹部非特异性症状或其他器官疾病的检查中意外发现的。影像学检查在肾癌的诊治过程的不同阶段均有重要的作用:对于原发肿瘤在于病灶的发现、定位、定性及分期;在术中可辅助定位;在术后及非手术治疗过程中是随诊的重要手段。不同的影像学检查方法在肾癌诊治中过程的不同阶段作用不同,应根据各方法的优劣和临床需要进行规范选择。
⒈胸部X线检查
肾癌患者应常规行胸部正侧位X线片,对胸部X线片有可疑结节或临床分期≥Ⅲ期的患者,需做胸部CT。
⒉超声检查
腹部超声检查是发现肾肿瘤最简便和常用的方法。肾超声造影检查有助于鉴别肾肿瘤良恶性,适用于慢性肾功能衰竭或碘过敏而不适宜行增强CT扫描的肾肿瘤患者以及复杂性肾囊肿患者的鉴别诊断。
(1)肾癌原发灶的诊断
1)灰阶与多普勒超声
超声检查经济、简便、无辐射,普及率高,为临床疑诊肾脏肿瘤的首选检查方法。临床上无症状肾癌多数为超声检查时发现。灰阶超声能够显示肿瘤大小、位置、与周围组织的关系。彩色多普勒超声(CDFI)能提供肿瘤的血供状态,亦能对静脉瘤栓的形成做出初步评价。灰阶超声及CDFI检查对囊实性肾肿瘤的鉴别有较高的敏感度。超声检查发现的Bosniak Ⅰ 型囊肿,临床可持续观察无需进一步检查。Bosniak Ⅱ型囊肿,每6~12月复查1次。若超声提示Bosniak Ⅲ和Ⅳ型囊肿及实性肾肿瘤,则建议超声造影、CT或MRI进一步检查。
2)超声造影
对于实性肾肿瘤,增强影像是鉴别良恶性病变最重要的手段,实时灰阶超声造影技术(CEUS)可提高血流检查的敏感度和准确度,对肿物早期动脉灌注和肿物微循环状态的提供更多的信息,对于检出及显示肾癌特征具有较高敏感度和特异度。CEUS诊断复杂肾囊肿(Bosniak ⅡF~Ⅲ)也具有很高的敏感度和特异度。
(2)肾癌术前分期
超声检查范围较局限,且易受成像分辨率、患者自身条件及操作者经验等影响,对肿瘤分期的准确度不如CT,故不推荐用于术前分期。
(3)肾癌术中诊断
超声由于无辐射及灵活便捷特点,除常规用于引导肿瘤穿刺活检,还经常用于术中探查以确定手术范围。术中检查能正确显示肾脏肿瘤,并对肿瘤与肾盂的关系及肾静脉、下腔静脉、右心房内瘤栓的范围作出清晰的判断。
⒊CT检查
腹部CT检查是肾癌术前诊断及术后随访的最常用检查方法。完整CT检查应包括平扫和增强扫描。CT扫描可对大多数肾肿瘤进行定性诊断,具有较高的诊断敏感度和特异度,因此经CT检查明确诊断而且拟行手术的患者无需术前穿刺证实。在CT扫描上肾透明细胞癌多具有较典型的对比剂“快进快出”表现:平扫多呈不均匀等/低密度的圆形、椭圆形肿块,增强后皮髓质期呈中-高度强化,肾实质期肿瘤密度低于肾实质呈低密度肿块。肿瘤内坏死、出血常见。但需注意的是,CT检查对部分少见类型肾癌与良性肿瘤如嗜酸细胞腺瘤和少脂型血管平滑肌脂肪瘤的鉴别仍有一定的困难。
除定性诊断外,CT检查还能为术前患者提供更多的诊断信息,包括:肿瘤的侵犯范围,包括静脉系统是否受侵(T分期),区域淋巴结是否转移(N分期),扫描范围邻近器官有无转移(M分期),有无变异血管(CTA)及双肾形态及功能的粗略评估等。
肾囊性肿物的Bosniak分类:肾脏囊性肿物为一组以囊性为主要表现的疾病,可为先天性、感染性、继发性或肿瘤性(良性及恶性)疾病。影像学表现可从单纯囊肿、略复杂囊性病变至复杂囊实性肿物。Bosniak以CT表现为基础,将肾囊性肿物分为4类,并根据不同级别提供临床处理意见(表6)。目前Bosniak分类中的Ⅰ、Ⅱ、Ⅳ类的诊断标准较为明确和处理意见亦比较适合,但部分ⅡF和Ⅲ类患者诊断敏感度和特异度仍比较低,仍需进一步研究补充。MRI或CEUS可能对这部分病变的诊断有所帮助。

⒋MRI 检查
腹部MRI检查是肾癌术前诊断及术后随访的较常用检查方法,可用于对CT对比剂过敏、孕妇或其他不适宜进行CT检查的患者。MRI对肾癌诊断的敏感度和特异度等于或略高于CT。MRI对肾静脉和下腔静脉瘤栓的显示诊断较CT更为准确,对肾脏囊性病变内结构的显示也较CT更为清晰,对于肾癌与出血性肾囊肿的鉴别诊断也比CT更具优势,因此是对于上述病变MRI可能是优于CT的更好选择。
⒌PET
目前,PET-CT检查临床应用最广泛的显像剂是18FDG,静脉注射后约50%未经代谢直接由肾脏排泄,会影响肾脏病变的显示;另一方面,Ⅰ~Ⅱ级肾透明细胞癌的细胞膜GLUT-1表达较低,且肾癌6-PO4-脱氧葡萄糖(FDG-6-PO4)分解酶过高,导致肾癌原发灶仅半数左右呈FDG代谢增高,另半数可与正常肾实质摄取无差异;因此18F-FDG PET-CT显像对肾癌原发灶的诊断价值有限,不推荐常规使用。其他新型的显像剂研究较多的是18F或11 C标记乙酸盐,对分化较好、恶性程度较低的肾癌有着良好的显像作用,可弥补单一18F-FDG显像的不足,但目前还处于研究阶段,没有做为常规检查。2018年的EAU和NCCN肾癌指南中也明确了PET不推荐用于肾癌的诊断和随访。但是,多项研究也表明PET-CT显像对肾癌的淋巴结转移和远处转移要优于传统影像检查方法,尤其在判断肾癌骨转移或骨骼肌转移方面更具优势,而且能够通过葡萄糖代谢变化早期监测疗效、预测患者的预后情况。2017年CSCO肾癌诊疗指南中提出PET或PET-CT可用于肾癌患者明确有无远处转移病灶,或需对全身治疗进行疗效评价的患者。
⒍核素骨显像
用于探查是否有骨转移以及转移灶的治疗随访。有骨痛等骨相关症状或血清碱性磷酸酶升高或临床分期≥Ⅲ期的肾癌患者,应行骨扫描检查明确是否有骨转移。核素全身骨显像发现骨转移病变可比X线片早3~6个月,当全身骨显像示可疑骨转移时,应对可疑部位进行局部断层融合显像或进行MRI、CT等检查验证。
⒎肾动态显像
核素肾动态显像能准确评价肾癌患者术前双肾和分肾功能,有助于指导手术方案的决策。
⒏肾肿瘤穿刺活检
经皮肾穿刺活检包括空芯针活检和细针穿刺(FNA),能为影像学不能诊断的肾肿瘤提供病理组织学依据。空芯针活检较FNA对诊断恶性肿瘤有更高的准确度,而两者结合可提高诊断准确率。具有实性成分的肾肿瘤首选空芯针活检。同轴技术可以通过同轴套管进行多次活检取材,避免潜在的肿瘤针道种植转移风险。取材应避开坏死区,至少获得2个质量良好的组织标本。若初次活检无结果,但影像学检查怀疑恶性时,则应考虑再次活检或手术探查。囊性肾肿瘤的空芯针活检诊断率和准确度较低,不推荐使用,除非内部有实性成分(Bosniak Ⅳ型囊肿)。对于复杂囊性肾肿瘤,空芯针活检和FNA联合可以相互补充结果。
穿刺风险及潜在扩散风险,尽管较低却不可忽视。经皮肾穿刺活检不适用于危重患者。对于拟手术患者,由于腹部增强影像诊断准确率很高,亦不推荐穿刺活检。不宜手术治疗的(年迈体弱或有手术禁忌)肾癌患者,或不能手术治疗的晚期肾癌患者,全身系统治疗前行肾肿瘤穿刺活检明确病理诊断(包括病理类型),有助于选择治疗用药。选择消融治疗的肾癌患者,应行肾肿瘤穿刺活检获取病理诊断。因此在实际工作中,仍需综合考虑穿刺风险、操作者技术水平以及是否可能影响到当前的治疗方案做综合决定。
五、晚期/转移性肾癌的预后评估
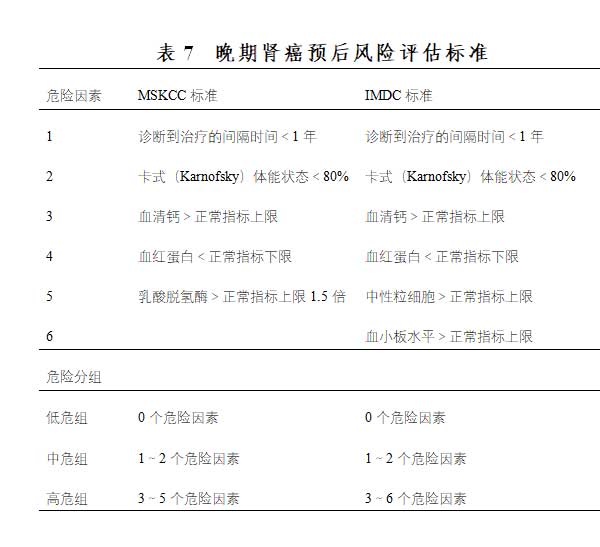
晚期肾癌的预后风险模型有助于患者危险分层和治疗选择,目前常用的包括纪念 Sloan Kettering 癌症中心(Memorial Sloan Kettering Cancer Center,MSKCC)标准和国际转移性肾细胞癌数据库联盟(International Metastatic Renal Cell Carcinoma Database Consortium,IMDC)标准(表7)。MSKCC评分建立在细胞因子时代,包括体力状态、乳酸脱氢酶、血红蛋白、血钙和自诊断到全身治疗时间5个危险因素,分为低危、中危和高危,相对应的中位总生存期为30个月、14个月和5个月。靶向治疗时代应用的IMDC评分,建立于MSKCC标准之上,包括MSKCC预后因素中4个(除外乳酸脱氢酶),又纳入血小板和中性粒细胞计数,低危、中危和高危患者中位总生存期分别为35.3个月、16.6个月和5.4个月。
六、治疗
肾癌患者通过影像学检查的结果确定肿瘤的临床分期(clinical stage grouping,cTNM),利用辅助检查评估患者对治疗的耐受能力,根据临床分期并结合患者的耐受力,选择恰当的治疗方式。对手术的患者依据病理学检查的结果确定病理分期(pathological stage grouping,pTNM),根据病理分期选择术后治疗及随诊方案。
(一)手术治疗
对于局限性和局部进展性肾癌患者而言,外科手术仍然是首选的可能使患者获得治愈的治疗方式。对于晚期肾癌患者,应以内科治疗为主,根据患者自身情况,可考虑同时采取减瘤性质的肾切除术,同时鼓励的转移病灶也可在充分评估后采取手术切除。
⒈根治性肾切除术
1963年Robson等建立了根治性肾切除术(radical nephrectomy,RN)的的基本原则,并确立了RN作为局限性肾癌外科治疗的“金标准”。经典的RN切除范围包括患肾、肾周筋膜、肾周脂肪、同侧肾上腺、从膈肌脚到腹主动脉分叉处淋巴结以及髂血管分叉以上输尿管。当前观念已发生变化,不推荐术中常规行肾上腺切除和区域淋巴结清扫。
(1)根治性肾切除术适应证:①局限性肾癌,无明确转移者;②肾静脉、下腔静脉瘤栓形成,无远处转移者;③肿瘤侵犯相邻器官,无远处转移,术前估计肿瘤可彻底切除者。
(2)根治性肾切除术的禁忌证:①晚期肾癌,全身广泛转移者;②肿瘤侵犯相邻器官,估计手术无法切除局部肿瘤者;③有严重出血性疾病者;④心、脑、肝、肺及循环系统有严重疾病,估计不能耐受麻醉和手术者。
(3)根治性肾切除术后并发症及处理
根治性肾切除术后,大约20%的患者会出现术后并发症,手术死亡率约2%。全身性并发症可发生于任何手术后,包括:心肌梗死、脑血管损伤、充血性心力衰竭、肺栓塞、肺不张、肺炎和血栓性静脉炎。充分的术前准备、避免术中低血压、适当补充血液和体液、术后呼吸训练、早期活动等均可减少这些并发症的发生。
在手术过程中应经常检查有无胃肠道损伤,如有撕裂伤必须修补并引流。肝撕裂伤可用褥式缝合法修补,脾脏损伤通常应行脾切除,小的撕裂伤可用牛皮胶原或氧化纤维素处理。行根治性左肾切除时可能会损伤胰腺尾部,最好的处理方法是行胰腺部分切除术。
术中未能发现的胰腺损伤可导致术后胰瘘的发生,这是一极为严重的术后并发症。通常术后早期即可发现,表现为急性胰腺炎的症状和体征,可从切口引流出碱性液体。腹部CT显示腹膜后间隙有液体积聚。应测定从切口引流出液体的pH和淀粉酶含量,并经皮或外科引流积聚液体以免形成胰腺假性囊肿或脓肿。经充分引流后多数瘘管可自行闭合,由于胰腺瘘管的愈合是一慢性过程,故需给患者高营养支持治疗。某些需要长期引流的患者应行外科治疗以闭合瘘管,方法为切除瘘管后行胰腺和空肠的Roux-en-Y吻合术。
其他可能发生的胃肠道并发症包括肠梗阻,患者出现肠鸣音,且肛门排气后方可进食,梗阻严重的患者需行胃肠减压。如果预计患者的梗阻时间会比较长或者患者的营养状况较差,则需考虑行胃肠外营养。
根治性肾切除术后可能会出现出血,表现为疼痛、出现休克体征、腹部或腰部肿胀以及切口或引流处有血液流出。出血可能源自肾蒂,但偶尔也可能是由于术中对邻近组织如脾、肝或肠系膜血管的无意损伤造成的。患者应根据需要进行输血和补液。大多数情况下,最好的方法是重新打开切口,清除血肿,修补出血部位。因凝血障碍而出现弥漫性出血时,可用纱布暂时填充伤口,并于24〜48小时后将其逐渐去除。
⒉保留肾单位手术
根治性肾切除术后患者仅剩一侧肾脏,可能会导致肾功能下降,增加慢性肾功能不全和透析的风险。慢性肾功能不全会增加患者发生心血管事件的风险,提高总体死亡率。对于局限性肾癌患者,如技术上可行,临床分期为T1a的肾癌患者,推荐行保留肾单位手术(nephron sparing surgery,NSS)。对于T1b期甚至T2期,也可考虑行NSS。手术中需要切除的肿瘤周围正常肾实质的厚度并非一个关键性的问题,只要保证最终手术标本切缘阴性。尽管肾部分切除术后会增加肿瘤局部复发的风险,但患者肿瘤特异性死亡率与根治性肾切除术相似。对于肾部分切除术的可行性,肿瘤的位置(外生型还是内生型)比肿瘤大小更为重要。肿瘤过大或位置过深,会增加肾脏手术时的热缺血时间,而且术后出血和尿漏的并发症风险也随之上升。因此,保留肾单位手术适应证也在一定程度上取决于外科医师的经验和手术技巧。
(1)NSS适应证包括:①绝对适应证:先天性孤立肾、对侧肾功能不全或无功能者以及双侧肾癌患者,根治性肾切除术将会导致肾功能不全或尿毒症。②相对适应证:肾癌对侧肾存在某些良性疾病,如肾结石、慢性肾盂肾炎或其他可能导致肾功能恶化的疾病(如高血压、糖尿病、肾动脉狭窄等)患者。③可选择适应证:临床分期T1a期(肿瘤≤4cm)或T1b期(肿瘤≤7cm),肿瘤位于肾脏周边,单发的无症状肾癌,对侧肾功能正常者可选择实施NSS。
(2)保留肾单位手术并发症及处理
1)出血:术中出现明显出血,主要原因是肾动脉阻断不全、肾脏异位动脉未阻断,或肾静脉开放,因此术前血管成像判断肾动脉分支和异位肾血管,术中强调完全阻断肾动脉,必要时同时阻断肾动静脉,可以减少术中出血。术中出血,微创手术时可以提高气腹压力、在原动脉阻断附近加用阻断夹子、寻找并阻断异位动脉、或动静脉同时阻断,必要时改为开放手术或者行根治性肾切除。开放手术术中出血,可以用无损伤血管钳再次阻断肾动脉、动静脉同时阻断、或缝合创面的出血位点止血,一般不需要改行根治性肾切除术。术后出血主要原因是术中集合系统和肾段动脉开放,又未完全缝合关闭,导致动脉出血至集合系统或肾脏周围。术后出血如局限于腹膜后,可能为自限性,也可以引起肉眼血尿。术后出血早期可以采取严密观察,卧床休息,连续观察血红蛋白和血细胞比容,随时监测生命体征和必要时输血。血管造影有助于确定肾段动脉活动性出血,并可通过血管内栓塞控制出血。严重的顽固性出血可能需要二次手术探查,寻找出血原因,并结扎活动性出血的血管或切除肾脏等。
2)漏尿:肾部分切术后出现引流管引流出尿液,往往在肾集合系统愈合后消失。如出现持续性引流时,多提示尿瘘形成。形成尿瘘的主要原因是术中集合系统开放,缝合过程中未完全闭合,或者缝合过深导致集合系统梗阻导致尿流不畅,以及血块堵塞集合系统造成集合系统梗阻。通过检测引流液中的肌酐水平,或血管内注射靛胭脂后观察引流液中是否出现染色,可以进一步明确。当尿路引流无明显梗阻时,大多数尿瘘可以自愈。当存在明显的肾积水或持续性尿外漏时,需放置输尿管支架。多数尿瘘通过适当的保守和干预治疗,数周内均可自愈,少数需二次手术闭合瘘管或切除肾脏。
3)肾功能不全:功能性或解剖性孤立性肾患者肾部分切除容易出现不同程度的肾功能不全。导致肾功能不全的原因是术中肾缺血,以及切除病变组织附近的部分正常肾组织。这种肾功能不全一般比较轻微,通过维持适当的水和电解质平衡可自愈。并且在大多数病例中,残余肾可通过代偿性增生来改善肾功能。严重的肾功能不全需行临时或长期血液透析,并在术前告知患者这种风险。
⒊手术相关问题
(1)开放手术 /腹腔镜手术/机器人辅助技术
与传统的开放性手术相比,腹腔镜手术的优点是微创手术切口小、损伤小、出血少、术后恢复快、合并症少、住院时间短,近期肿瘤控制率与开放手术无明显差异。缺点是器械昂贵、技术较复杂、熟练掌握的学习曲线较长、初学阶段手术时间较长。随着技术的熟练,手术时间会明显缩短,切除的彻底程度则可达到与开放手术完全相同。达芬奇机器人的问世,使得腹腔镜手术最难的手术环节——腔内缝合重建,被大大简化。这项进步使得腹腔镜肾部分切除术的几个手术关键步骤变得更容易掌握,学习曲线更快。目前,在技术条件允许的情况下,开放手术、腹腔镜手术或机器人辅助技术均可应用于肾癌患者的外科手术治疗,怎样选择很大程度上取决于肾肿瘤的大小和位置,以及外科医师的经验程度。
(2)同侧肾上腺切除
经典的根治性肾切除术的范围包括同侧肾上腺。但是鉴于较小的肾癌累及同侧肾上腺的风险很低,因此,临床上只有较大的肾肿瘤或位于肾上极的肿瘤在行根治性肾切除术时才会同时切除同侧肾上腺。尽管对是否保留或切除病灶同侧肾上腺仍有争议,但在CT扫描未见肾上腺异常的前提下,术中应考虑保留同侧肾上腺。
对符合下列4个条件的患者,行根治性肾切除术时常选择保留同侧肾上腺:①临床分期为Ⅰ或Ⅱ期;②肿瘤<8cm;③肿瘤位于肾中、下部分;④术前CT显示肾上腺正常。如手术中发现同侧肾上腺异常,应当予以切除。
(3)区域淋巴结清扫
在行根治性肾切除术时是否需要行腹膜后区域淋巴结清扫术也存在争议。当前尚无证据表明淋巴结清扫能够使患者获益。欧洲癌症研究与治疗组织(EORTC)20年随机对照Ⅲ期临床研究结果显示,对于可切除的局限肾癌(N0M0)行淋巴结清扫与不行淋巴结清扫,2组无疾病进展生存、疾病进展时间和总生存率差异无统计学意义。因此,肾癌患者在行根治性肾切除术时,一般不常规进行区域或广泛淋巴结清扫。若术前影像学检查显示区域淋巴结肿大或术中触及肿大淋巴结,可行区域淋巴结清扫术或切除以明确病理分期。
(4)肿瘤切缘阳性的处理
肾部分切除术患者最担心的是肿瘤复发的问题。肾部分切除术后同侧肾脏肿瘤复发率在1%∼6%,多由于原发肾癌的多灶性或切缘阳性所致。对于肾部分切除术的手术切缘阳性是否会增加患者肿瘤复发的风险以及对预后的影响仍存有争议。研究表明即使肾部分切除术切缘阳性,中期随访结果显示也未见患者肿瘤复发增加。甚至一些研究表明术后立即或后来对患者行补救性肾切除术时,绝大多数都未发现肿瘤残留的迹象。文献报告3%∼8%的NSS会出现术后病理切缘阳性(PSM),但只有那些病理分级较高(Ⅲ~Ⅳ级)的患者术后复发风险增高。
(5)静脉癌栓的处理
肾癌患者中约有10%伴随肾静脉或下腔静脉癌栓,肾癌静脉瘤栓的分级法常采用美国梅奥医学中心的五级分类法(表8)。由于静脉癌栓的外科手术治疗伴随较大的风险及并发症,因此术前需要进行全面准备的评估,制定详细的治疗方案,并且需要有经验的团队进行手术。
评估:术前进行增强MRI或CT扫描及血管成像,了解静脉癌栓的范围及程度、有无静脉管壁侵犯等,以制订进一步手术治疗方案。
手术:伴有静脉癌栓的局部晚期肾癌的手术方式根据静脉癌栓的程度不同,手术细节有所区别。手术第一步为分离血管。在主动脉根部结扎肿瘤侧肾动脉,然后控制静脉及取出癌栓。为了更好的控制出血及肿瘤暴露,可以将下腔静脉的分支血管(腰静脉、小分支肝静脉等)进行结扎。为了保证静脉回流的通畅,切忌将所有的分支血管全部结扎。术中尽量少触碰肾脏及肿瘤,以减少癌栓脱落风险。局限于肾静脉的癌栓或癌栓刚进入到下腔静脉的肾癌的手术与常规的根治性肾切除手术类似。当癌栓处于肾静脉开口与肝静脉之间时,手术时在癌栓上方和下方分别阻断下腔静脉,同时需要阻断对侧肾静脉。通常情况下,不需要采用血液分流技术。在下腔静脉前方切开血管,将肾脏及肿瘤、同侧肾静脉和静脉癌栓一并切除。仔细检查及冲洗下腔静脉内壁,以避免肿瘤残留。当癌栓处于肝静脉与膈肌之间时,需要采用血液分流技术,根据术中所需要阻断下腔静脉的程度及引起的血流动力学改变的状况,决定采用何种分流技术。
预后:静脉癌栓的程度与生存预后的关系目前尚无明确定论。一项纳入422例病例的回顾性研究结果显示,伴有下腔静脉癌栓患者的生存预后差于癌栓局限于肾静脉的患者。另一项研究显示,癌栓侵犯肾静脉管壁的预后差于无管壁侵犯的患者。Blute等报道,没有远处转移及淋巴结转移的静脉癌栓肾癌患者,未进行术后辅助治疗的情况下,中位生存时间为3.1年,5年生存率为59%。

(6)T4期肾癌的处理
肾癌侵犯至肾筋膜外并累及周围脏器时,为T4期肿瘤。可累及升结肠、十二指肠、降结肠、胰腺、膈肌、肝脏、脾脏、肾上腺、输尿管等。早年研究表明,T4期肿瘤手术效果差,不建议行手术治疗。但后续一些研究表明,T4期肾癌手术可以使患者获益。MDACC研究报道,30例术前临床分期为T4NxM0患者接受手术治疗,术中切除肿瘤及受侵犯的邻近脏器,切缘均为阴性。60%患者的分期出现降期现象,其中2例患者病理分期为T2期。多因素回归分析结果显示,pT4及淋巴结转移为生存预后的独立预测因素。淋巴结阴性患者的3年总生存率为66%,而淋巴结转移患者的3年总生存率为12%。此项研究表明术前及术中的分期并不完全准确,相当一部分患者会存在分期高估现象。因此,对于临床局部分期为T4且没有远处转移的患者,如果身体状况允许,围手术期风险可控的情况下,可考虑进行手术治疗。MSKCC的研究报道,在病理分期为T3或T4期联合邻近脏器切除的肾癌患者中,约四分之一患者存在淋巴结转移,绝大多数患者切缘阴性(36%切缘阳性)。切缘阳性患者的生存时间明显缩短。全组患者的中位生存时间为11.7个月。Capitanio回顾性分析SEER数据库中临床分期为T4N0-2M0的肾癌,246例接受手术,64例未接受手术。手术组的患者中位生存时间为48个月,而未手术组患者的中位生存时间为6个月。手术组中125例病理分期T4N0的患者,10年肿瘤特异性死亡率为40%。然而在淋巴结转移的患者中,并未见到明显获益。在处理临床T4期肾癌患者时,由于涉及邻近脏器的切除与重建,因此多学科协作治疗十分重要。综上所述,对于临床T4N0M0的肾癌患者,如果条件允许,积极手术可能会给患者带来明显获益。
(二)介入治疗
⒈栓塞治疗
(1)肾动脉栓塞
肾动脉栓塞术可用于肾肿瘤的姑息性治疗,以缓解临床症状、提高生存质量。
1)适应证:①肾肿瘤所致疼痛;②肾肿瘤相关出血性事件,如肾肿瘤破裂出血、血尿等;③部分巨大、富血供肾脏肿瘤的外科术前栓塞:由于其对延长患者生存时间、减少术中出血及降低术后并发症等方面获益尚不明确,因此不推荐常规使用。
2)禁忌证:①无法纠正的凝血功能障碍;②严重感染;③外周血白细胞和血小板显著减少(非绝对禁忌,如脾功能亢进者):白细胞<3.0×109/L,血小板<50×109/L;④严重肾功能障碍。
3)操作程序要点:①肾动脉造影,通常采用Seldinger方法,经皮穿刺股动脉或桡动脉插管,导管置于肾动脉行DSA造影,必要时可行肾上腺动脉造影,寻找侧支供血。②仔细分析造影表现,明确肿瘤的部位、大小、数目以及供血动脉。③超选择至肿瘤供血动脉进行栓塞,注意保留正常肾单位。④非透明细胞癌,可考虑肾动脉化疗栓塞术,常用药物有吉西他滨、氟尿嘧啶、卡培他滨、顺铂等;而新型化疗药物,如洛铂等,具有毒性较低等特点,在肾癌的化疗栓塞中也得到了逐步应用。
4)术后并发症:栓塞后综合征,是肾动脉栓塞术后最常见不良反应,主要表现为发热、疼痛、恶心和呕吐等。发生原因是肝动脉被栓塞后引起局部组织缺血、坏死。此类不良反应可持续5∼7天,经对症治疗后大多数患者多可完全恢复。
(2)肺转移灶栓塞
肺是肾肿瘤最常见的转移部位,部分肾肿瘤患者以咯血为首发症状。支气管动脉栓塞术可用于治疗肺转移灶,防治肺转移灶相关并发症,提高生存质量。
1)适应证:①肺转移灶所致疼痛,如胸膜转移等;②肺转移灶所致呼吸困难,如气道受压狭窄;③肺转移灶相关出血性事件,如咯血、血胸等。
2)禁忌证:①无法纠正的凝血功能障碍;②严重感染;③外周血白细胞和血小板显著减少(非绝对禁忌,如脾功能亢进者):白细胞<3.0×109/L,血小板<50×109/L;④严重肾功能障碍。
3)操作程序要点:①支气管动脉造影,通常采用Seldinger方法,经皮穿刺股动脉或桡动脉插管,导管置于支气管动脉行DSA造影,贴邻或位于胸膜者必要时可行肋间动脉等造影,寻找侧支供血。②仔细分析造影表现,明确肿瘤的部位、大小、数目以及供血动脉。③超选择至肿瘤供血动脉进行栓塞,注意避开脊髓动脉。④转移性非透明细胞癌,可考虑支气管动脉化疗栓塞术。
4)术后并发症:栓塞后综合征,是支气管动脉栓塞术后最常见不良反应,主要表现为发热、疼痛、咳嗽、咯血等。发生原因是肝动脉被栓塞后引起局部组织缺血、坏死。介入治疗术后的不良反应会持续5∼7天,经对症治疗后大多数患者可以完全恢复。
(3)肝转移灶栓塞
肝脏也是肾肿瘤的常见转移部位之一。选择性肝动脉栓塞术可用于治疗肝转移灶,防止肝功能恶化,提高生存质量。
1)禁忌证:①无法纠正的凝血功能障碍;②严重感染;③外周血白细胞和血小板显著减少(非绝对禁忌,如脾功能亢进者):白细胞<3.0×109/L,血小板<50×109/L;④严重肾功能障碍;⑤严重肝功能障碍(Child-Pugh C级),包括黄疸、肝性脑病、难治性腹水或肝肾综合征。
2)操作程序要点:①肝动脉造影,通常采用Seldinger方法,经皮穿刺股动脉插管,导管置于腹腔干或肝总动脉行DSA造影,造影图像采集应包括动脉期、实质期及静脉期;应做肠系膜上动脉造影、注意寻找侧支供血。②仔细分析造影表现,明确肿瘤的部位、大小、数目以及供血动脉。③肝动脉栓塞:超选择至肿瘤供血动脉进行栓塞。④转移性非透明细胞癌,可考虑肝动脉化疗栓塞术。
3)术后并发症:栓塞后综合征,是肝动脉栓塞术后最常见不良反应,主要表现为发热、疼痛、恶心、呕吐、一过性肝功能异常等。发生原因是肝动脉被栓塞后引起局部组织缺血、坏死。介入治疗术后的不良反应会持续5∼7天,经对症治疗后大多数患者可以完全恢复。
⒉消融治疗
近年来广泛应用的消融治疗,具有创伤小、疗效确切的特点,使一些不接受或不耐受手术切除的肝癌患者亦可获得根治的机会。
消融治疗是借助医学影像技术的引导对肿瘤靶向定位,局部采用物理或化学的方法直接杀灭肿瘤组织的一类治疗手段。肾肿瘤及寡转移灶的消融手段主要包括射频消融和冷冻消融。消融治疗最常用超声引导,具有方便、实时、高效的特点。CT及MRI结合多模态影像系统可用于观察超声无法探及的病灶。CT及MRI引导技术还可应用于肺、肝脏、肾上腺、骨等转移灶的消融等。
(1)射频消融
射频消融的路径通常分为经皮消融和经腹腔镜消融,在T1a期肾肿瘤患者中,二者术后并发症发生率、复发率及肿瘤特异性生存率没有差异。在T1a期肾肿瘤患者中,射频消融与部分肾切除术相比较,二者总生存率及肿瘤特异性生存率均没有差异,射频消融的并发症发生率及输血率均低于部分肾切除术,射频消融的局部复发率高于部分肾切除术但二者远处转移率没有差异。
(2)冷冻消融
冷冻消融的路径通常分为经皮消融和经腹腔镜消融,二者总生存率、肿瘤特异性生存率、无复发生存率及并发症发生率没有差异,经皮消融住院时间短于经腹腔镜消融。冷冻消融与部分肾切除术相比较,部分研究显示二者总生存率、肿瘤特异性生存率、无复发生存率、无病生存率、局部复发率及远处转移率没有差异,部分研究显示在以上指标中部分肾切除术优于冷冻消融。
射频消融与冷冻消融在总生存率、肿瘤特异性生存率、无复发生存率及并发症发生率没有差异。
消融治疗适应证:①T1a期中,高龄或伴有合并症者;②Ⅳ期中原发病灶潜在切除可能伴寡转移,不可手术者;③复发或Ⅳ期中不可切除者,在一线治疗基础上可联合寡转移灶消融术;④不接受或不耐受外科手术者;⑤需尽可能保留肾单位者;⑥肾功能不全者;⑦存在全身麻醉禁忌者。
消融治疗禁忌证:①无法纠正的凝血功能障碍;②严重感染;③外周血白细胞和血小板显著减少(非绝对禁忌,如脾功能亢进者):白细胞<3.0×109/L,血小板<50×109/L。
操作程序要点:①消融前需穿刺活检,为后续治疗及随访提供支撑;②治疗前应该全面而充分地评估肿瘤的大小、位置、数目等;要注意肿瘤与邻近器官的关系,制定合理的穿刺路径及消融范围,在保证安全的前提下,达到足够的安全范围;③根据肿瘤的大小、位置,选择适合的影像引导技术(超声或CT)和消融手段(射频或冷冻);④消融范围应包括5mm的癌旁组织,以获得“安全边缘”,彻底杀灭肿瘤,对于边界不清晰、形状不规则的浸润型癌或转移癌灶,在邻近肝组织及结构条件许可的情况下,建议适当扩大消融范围。
术后并发症:发热、疼痛、出血、感染等,大部分为轻度。经对症治疗后大多数患者可以完全恢复。
(3)其他技术
其他肾脏肿瘤消融治疗方法主要包括:微波消融、高强度超声聚焦消融、不可逆电穿孔及高低温复合式消融等。以上方法在肾癌的消融治疗中也得到了逐步应用。
(三)主动监测
主动监测(Active surveillance,AS)是指通过定期进行腹部影像学检查,监测肾肿瘤的大小变化,在随诊期间一旦出现肿瘤进展则接受延迟的干预治疗。等待观察(Watchful waiting,WW)与主动监测不同,是指患者具有较严重的合并症,不适合主动治疗,等待观察直到出现相关症状再对症处理,不需要定期影像学检查。
一项针对小肾肿瘤的多中心前瞻性注册研究DISSRM(Delayed Intervention and Surveillance for Small Renal Masses)显示主动监测与主动治疗相比,小肾肿瘤患者的2年总生存率相似,分别为98%和96%;5年总生存率主动监测组略低,分别为92%和75%(P=0.06);7年总生存率主动监测组较差,分别为91.7%和65.9%(P=0.01)。但在肿瘤特异性生存率方面,主动监测与主动治疗相比在5年(99%对100%,P=0.3)及7年(99%对100%,P=0.5)均没有差异。AS组患者的年龄更大,ECOG评分更差,合并症更严重,肿瘤更小,多发及双肾肿瘤比例更高。
对于大多数小肾肿瘤(small renal masses,SRMs,肿瘤最大径 ≤ 4 cm)中的高龄及合并症多的患者来说,手术麻醉及其他合并症所带来的风险,往往高于肿瘤本身。前瞻性研究显示:AS组SRMs患者的5年总生存率53%∼90%,5年肿瘤特异性死亡率0.2%∼1.9%,5年无进展生存率97%∼99%。AS是老年或体弱SRMs患者的可行选择。美国泌尿外科学会(AUA)在 2009 年发布的关于 T1 期肾肿瘤诊疗指南中便提出 AS 可作为存在高危手术因素及合并症者的治疗方案。2017年美国临床肿瘤学会(ASCO)推荐 AS 可作为存在高危因素及预期寿命不佳小肾肿瘤患者的首选治疗方案,并明确了其适用范围,绝对适应证:存在较高手术麻醉风险或预期寿命 <5 年;相对适应证:如治疗可致终末期肾病风险,SRM<1 cm 或预期寿命 <10 年。但对于年轻无合并其他疾病 SRMs的患者不主张行长期 AS。
(四)药物治疗
自2005年索拉非尼被批准用于转移性肾癌的治疗以来,转移性肾癌的治疗进入了靶向治疗时代。至今美国食品药品管理局(FDA)已先后批准了十余种药物及方案用于转移性肾癌的治疗。这些药物从作用机制方面主要分为:①抗VEGF/VEGFR途径,主要包括舒尼替尼、培唑帕尼、索拉非尼、阿昔替尼、卡博替尼、仑伐替尼、贝伐珠单抗等;②抑制mTOR途径:包括依维莫司和替西罗莫司;③免疫检查点抑制剂:包括伊匹单抗;④程序性死亡受体抑制剂:包括纳武单抗;⑤其他:包括细胞因子(白介素-2和IFN-α)及化疗(吉西他滨和多柔比星)。化疗主要作为具有肉瘤样分化的转移性肾癌患者的治疗,集合管亚型和髓质亚型也考虑化疗。
联合用药方案主要包括贝伐珠单抗+IFN-α、纳武单抗+伊匹单抗(适用于中-高风险晚期透明细胞为主型肾细胞癌)、仑伐替尼+依维莫司(适用于晚期透明细胞为主型肾细胞癌的二线治疗)、贝伐珠单抗+厄洛替尼(适用于部分进展性乳头状肾细胞癌,包括HLRCC患者)、贝伐珠单抗+依维莫司(适用于部分进展性乳头状肾细胞癌,包括HLRCC患者)、仑伐替尼+依维莫司(适用于晚期非透明细胞为主型肾细胞癌)等。
目前国内已批准用于晚期肾癌治疗的药物包括培唑帕尼、舒尼替尼、阿昔替尼、索拉非尼、依维莫司、白介素-2、IFN-α等。
(五)中医中药治疗
中医药有助于促进肾癌术后机体功能恢复,减少免疫治疗及靶向药物治疗的不良反应,缓解患者症状,改善患者生活质量,可能延长生存期,可以作为肾癌治疗的手段之一,可单独应用或与其他抗肿瘤药物联合应用。
我国药监部门曾经批准的治疗肾癌的现代中药制剂不多,目前上市的中药制剂包括百令胶囊、消癌平等药物在内,治疗适应证多针对多种肿瘤,其中也包括治疗肾癌,但是这些药物已上市多年,早期的实验和临床研究比较薄弱,尚缺乏高级别的循证医学证据加以充分支持,需要积极进行深入研究。
除了这些上市的中成药外,遵从中医辨证论治原则采用中药复方治疗是中医最常用的方法之一,可根据患者个体差异,开展个体化治疗,具有一定优势;在减轻肿瘤相关并发症,改善患者生活质量,延长患者生存方面有一定的疗效。
(六)放疗
肾癌是一种对常规放疗不敏感的肿瘤,以往针对高危肾癌术后放疗的临床研究显示辅助放疗没有生存获益,因此不建议根治术后做辅助性放疗。
放疗主要用于肾癌的姑息治疗,如对局部瘤床复发、区域或远处淋巴结转移、骨骼、脑或肺转移患者做姑息放疗,达到缓解疼痛、改善生存质量的目的。
近10多年来放疗技术迅速发展,在一些回顾性和临床I期或Ⅱ期的研究中,应用立体定向放射治疗(Stereotactic body radiation therapy,SBRT,即单次大剂量照射一次或数次的分割照射模式)技术逐渐用于治疗肾癌。回顾性分析显示:SBRT可以取得优于常规放疗的治疗效果。在一些回顾性和临床I期或Ⅱ期的研究中,SBRT取得了很好的近期局控率,并具有良好的治疗安全性。但报道的病例数均较少,且缺乏长期随访的结果。目前尚无随机分组研究证明SBRT疗效优于常规分割放疗或其他局部治疗手段。所以SBRT只能在有精准放疗技术支持的和具备丰富放疗经验的医师及物理师的医疗中心,作为可供选择的一种肾癌姑息治疗的手段,或开展相关的临床研究。
(七)靶向药物常见不良反应及处理
⒈高血压:是靶向药物治疗最常见的毒性反应之一,为血管内皮生长因子或血管内皮生长因子受体(vascular endothelial growth factor receptor,VEGFR)抑制剂类药物共同的不良反应(表9)。文献报道VEGFR酪氨酸激酶抑制剂类药物治疗相关高血压的发生率为24%~40%,其中8%~16%的患者为Ⅲ级以上高血压。国内报道的发生率与国外类似,所有级别高血压的发生率为15%~37%。开始靶向治疗前应评估基线血压,对于原有高血压的患治疗期间目标血压应控制在140/90mmHg以下。当高血压达到Ⅱ级以上或I级伴有症状时,必须用药物控制。降压药物最好选择血管紧张素转换酶抑制剂。避免应用抑制CYP3A4的钙离子拮抗剂,以免产生药物间相互作用,如果需要与影响CYP3A4的药物同时给药,则应考虑调整药物剂量。在治疗间隔期,要暂停或降低降压药剂量并严密监测血压。

⒉血液学毒性:晚期肾癌靶向治疗常见的血液学毒性为中性粒细胞减少、血小板减少和贫血(表10)。舒尼替尼引起的血液学毒性的发生率较高,也是导致中国患者减量或停药的主要原因。治疗前和治疗期间需定期监测血常规,注意感染症状。若中性粒细胞减少≥I级,应给予升白细胞药物直至升至正常水平为止。对于血小板减少,可采取常规升血小板治疗。患者出现头晕、视物模糊、气促或其他贫血症状时应予以重视,必要时给予维生素B12和铁剂。出现I级以上血液学毒性时需减少靶向药物剂量。Ⅲ/Ⅳ级血液学毒性应停药,直至血液学毒性降低至基线水平后再重新开始治疗。若患者在常规治疗期间Ⅲ/Ⅳ级血液学毒性迅速恢复,则无需调整剂量,但需密切监测,同时可考虑调整给药方案。

⒊手足综合征与皮肤毒性:手足综合征(hand—foot syndrome,HFS)通常表现为双侧掌跖皮疹,伴疼痛和感觉迟钝,受机械牵拉的部位易出现过度角化、红斑和脱屑(表11)。文献报道索拉非尼引起的HFS发生率较高,所有分级HFS的发生率为51.0%,≥Ⅲ级的HFS发生率为16.1%。中国患者的手足皮肤反应更为常见,文献报道所有级别HFS发生率为55%~68%。皮肤毒性的临床表现为干皮、皮疹、瘙痒、水疱、蜕皮、皮肤角质局部增厚,或脂溢性皮炎伴皮肤松垂。通常出现于治疗开始后3∼8周。在靶向治疗中,所有分级皮疹的发生率为13%∼37%,HI级以上症状为0.1%~4.0%治疗前检查手掌和足底,排除原有的皮肤角化区域。症状出现时应立即干预,可采用含有10%尿素组分的油膏或乳液;如果出现过度角化,则使用含有35%~40%尿素的油膏进行去角质治疗。出现Ⅱ级以上的症状可使用含0.05%氯倍他索软膏;若伴有疼痛,可使用局部镇痛药如2%利多卡因。若出现严重症状,建议请皮肤科会诊。当发生Ⅱ级以上的HFS时,可以考虑中断给药,直至症状严重程度缓解至低于I级,减量或以相同的剂量重新开始治疗。

⒋胃肠道不良反应:常见腹泻、恶心和呕吐(表12),轻度腹泻可以补充电解质,发生重度腹泻应静脉输液和补充电解质,同时可用洛哌丁胺、地芬诺酯等药物。服用质子泵抑制剂或H2受体拮抗剂可能有利于预防和恶心症状相似的消化不良。止吐治疗建议使用多巴胺拮抗剂,如甲氧氯普胺或阿立必利。胃肠道不良反应与饮食习惯有关,建议患者少量多餐,保证足够量的液体摄入,清淡饮食,忌辛辣,避免使用泻药,避免使用高渗食物添加剂。对于I级和Ⅱ级胃肠道不良反应通常无需调整靶向药物剂量;在出现Ⅲ级和Ⅳ级不良反应时,应减量或停药。

⒌甲状腺功能减退:使用VEGFR抑制剂治疗的晚期肾癌患者中有12%~19%出现不同程度的甲状腺功能减退(表13),且发生率随治疗时间的延长而逐渐增加。国内研究结果显示甲状腺功能减退的发生率略高于西方人群,为14.0%~24.9%。部分患者可能发生暂时性的甲状腺功能亢进,一般无需干预,在随后的治疗中大部分会发展为甲状腺功能减退。肾癌靶向治疗的甲状腺功能减退分级见表13。在治疗初始时对患者进行甲状腺功能检查,并且在靶向治疗期间密切监测甲状腺素及促甲状腺激素(thyroid stimudating hormone,TSH)。不伴症状的TSH轻度升高,只需继续监测即可。TSH>10 mU/L或者出现甲状腺功能减退临床症状的患者,需用甲状腺激素替代治疗。大多数情况下,甲状腺激素替代治疗可有效控制症状,不需要暂停靶向药物治疗或调整剂量。

⒍肝脏毒性:在使用培唑帕尼治疗时,应密切监测肝功能。对于肝功能损害患者,建议应用保肝药物,对于有可能出现肝脏损害的患者,在开始靶向治疗前要针对原发肝脏疾病积极治疗(例如乙型肝炎、肝硬化等)。在治疗期间,若发生ALT上升至>8×ULN时,应及时停药,待恢复至基线水平再恢复治疗;恢复治疗后若再次发生ALT上升至>3×ULN的情况,应永久停药;若并发ALT上升至>3×ULN和胆红素上升至>2×ULN时,应永久停药。
⒎间质性肺病(interstitial lung disease,ILD):是一组主要累及肺间质、肺泡或细支气管的肺部弥漫性疾病,在二线药物mTOR抑制剂治疗中发生率较高,为19.8%。使用mTOR抑制剂治疗期间尤其要注意合并ILD和感染的情况,应慎用于双肺多发性转移、肺功能较差、阻塞性肺炎或其他活动性感染患者。开始治疗前,在有呼吸道症状的晚期肾癌患者中应进行评估,并定期监测肺部影像检查及肺功能。较轻的ILD无需采取措施,密切监测即可。严重ILD,应停止靶向药物治疗,并用激素(如甲泼尼龙)冲击治疗。
⒏心脏毒性:VEGFR抑制剂引起的心脏不良事件发生率为2%~10%,表现为左室射血分数(1eft ventricular ejection fraction,LVEF)下降、心肌缺血等。对于无心脏危险因素的患者,应考虑进行基线LVEF检测。有心脏危险因素或近期发生过心血管不良事件的患者,应密切监测生命体征和LVEF。若发生充血性心力衰竭,应暂停靶向治疗;若未发生症状明显的充血性心力衰竭,但LVEF<50%,或较基线LVEF值下降20%,应减少靶向药物剂量或暂停治疗。既往有QT间期延长病史、服用抗心律失常药物、心动过缓、电解质异常等患者,应定期进行心电图检查和血钾、血镁检测。
(八)局限性肾癌的治疗
局限性肾癌(localized renal cell carcinoma)是指肿瘤局限于肾脏被膜内,包括TNM分期为T1~2N0M0期,临床分期为Ⅰ、Ⅱ期的肾癌。随着影像学技术的提高和健康体检的普及,局限性肾癌所占的比例已经超过50%。越来越多的研究显示在大多数T1期,部分T2期,甚至少部分T3a期肾细胞癌中,肾部分切除术与根治性肾切除术具有相似的肿瘤学结果,和更好的肾功能保护。
对T1a期肾癌患者,在技术允许的情况下均推荐首选保留肾单位手术,对于解剖结构复杂难以实行肾部分切除术且对侧肾功能正常者可行根治性肾切除术。开放手术、腹腔镜或机器人等辅助技术均可用于开展肾部分切除术或根治性肾切除术。对于不能接受或耐受手术的T1a期肿瘤患者可以选择消融治疗,存在高危因素及预期寿命不佳者的可推荐主动监测;对T1b期肾癌患者推荐采用保留肾单位手术或根治性肾切除术,在手术方式的选取上仍旧需要考虑肿瘤的复杂性,如肿瘤大小、位置、深度以及患者的个体差异等。T2期肾癌患者首选根治性肾切除术,部分有临床需求的合适患者也可以选择PN。
术后辅助治疗:局限性肾癌手术后辅助的放、化疗,免疫治疗及靶向治疗均不能降低肿瘤的复发率和转移率。因此,T1~2N0M0期肾癌患者术后以随诊观察为主,不常规使用辅助治疗。
(九)局部进展期肾癌的治疗
局部进展性肾癌(locally advanced renal cell carcinoma)是指肿瘤突破肾脏被膜,累及肾周脂肪或肾窦脂肪但仍局限于肾筋膜内,可伴有区域淋巴结转移和(或)静脉瘤栓,无远处转移的肾癌,包括TNM分期为T1~2N1M0/ T3N0~1M0期的肾癌,临床分期为Ⅲ期。
局部进展性肾癌首选根治性肾切除术,肾部分切除术仅在技术上可行且有临床需求的特定患者施行。近来的一些回顾性或前瞻性Ⅱ期研究显示T2~T3期肾癌行术前新辅助靶向治疗,具有一定的缩瘤效果,可试用于局部切除困难的cT3期肿瘤,但尚缺乏高水平的研究证实。
根据病变程度和患者的身体状况,选择是否切除区域淋巴结或血管瘤栓。①淋巴结清扫术:局部进展性肾癌患者行区域或扩大淋巴结清扫术,对影像淋巴结阴性者(cN0)只对判定肿瘤的分期有意义,并不提高患者的生存率。而对淋巴结阳性(cN+)的患者,可行淋巴结清扫术,但淋巴结清扫术只对少部分患者有益,且清扫的范围仍有争议。②肾静脉和(或)腔静脉瘤栓的外科治疗:对于没有远处转移的肾癌合并静脉瘤栓患者,如技术上可行,应争取手术切除患肾及瘤栓。肾癌静脉瘤栓的长度以及瘤栓是否浸润腔静脉壁与患者的预后关系密切。肾静脉或腔静脉瘤栓取出术死亡率约为9%。③对于肾上极的大肿瘤、术前影像学或术中探查发现肾上腺肿瘤的患者应一并切除患侧肾上腺。
局部进展性肾癌术后辅助治疗:对于局部进展性肾癌术后尚无标准的辅助治疗方案,首先推荐加入临床试验,否则给予观察随诊。在局限高危的透明细胞肾癌患者,一项随机、双盲,安慰剂对照的3期临床研究(S-TRAC trial),入组615例高危透明细胞肾癌[Ⅲ~Ⅳ期和(或)区域淋巴结转移],服用sunitinib(50 mg/d,4/2)或 placebo(4/2)持续1年。与安慰剂相比,辅助舒尼替尼可以延长局限高危肾透明细胞癌术后患者的无病生存期(DFS 6.8年 vs. 5.6年,HR 0.76,P=0.03)。2017年11月,舒尼替尼成为首个被FDA批准用于具高危复发风险RCC患者的术后辅助治疗药物。
(十)晚期/转移性肾癌的治疗
晚期/转移性肾癌指肿瘤已突破肾筋膜,伴区域外淋巴结转移或远处转移,包括TNM分期为T4N0~1M0/ T1~4N0~1M1期,临床分期为Ⅳ期的肾癌。
以全身药物治疗为主,辅以原发灶或转移灶的姑息手术或放疗。转移性肾癌的治疗需全面考虑原发灶及转移灶的情况、肿瘤危险因素评分及患者的体能状况评分,选择恰当的综合治疗方案。
⒈外科治疗
外科手术作为转移性肾癌的辅助性治疗手段,包括原发灶的减瘤手术以及转移灶的姑息性切除。少数患者可通过外科手术获得较长期生存。
(1)肾原发病灶的外科治疗
外科减瘤术应在有效的全身治疗基础上进行。对低危险因素且体能状态良好的患者应行减瘤性肾切除术,减瘤手术可提高IFN-α或(和)IL-2治疗的疗效,延长患者的生存期5个月左右。回顾性研究显示,减瘤性肾切除(CN)及转移灶切除在肾癌的靶向治疗时代仍可能带来生存获益。目前实施减瘤性肾切除术较适用于一般情况良好(ECOG评分<2)、无或轻微相关症状,转移负荷低、手术能显着降低肿瘤负荷的mRCC患者。此外,对肾肿瘤引起严重血尿或疼痛的患者,可行姑息性肾切除术或肾动脉栓塞,以缓解症状、提高患者的生存质量。合并脑转移者预后差,通常不建议全身治疗前接受减瘤性肾切除。减瘤性肾切除
(2)转移灶的外科治疗
对孤立性转移瘤,若患者的行为状态良好,可手术切除转移灶。肺是肾癌最常见的转移部位,单发肺转移或转移灶位于一叶肺,手术切除可能有助于延长患者的生存期。骨也是肾癌常见的转移部位,外科手术可用于切除转移灶,或预防和治疗骨相关事件。对原发病灶已切除或可切除,且只有单一骨转移的患者,应进行积极的外科治疗。承重骨伴有骨折风险的患者首选外科治疗,应进行预防性内固定,避免骨相关事件的出现。已出现病理性骨折或脊髓的压迫症状的患者,若预计患者存活期>3个月、体能状态良好、手术能改善生活质量,也应行手术治疗。转移灶切除的有利因素包括肾切除至转移灶发现≥1年、单发转移、转移灶能完全切除、单纯肺转移、年龄≤60岁。
在靶向治疗时代,靶向药物治疗以及减瘤性肾切除术在mRCC中的应用价值目前还有待进一步探讨。SURTIME研究已经初步证明靶向药物治疗后再序贯进行减瘤性肾切除可改善总生存,并能降低直接手术造成的相关并发症发生率和死亡率;而CARMENA研究则证实对于可接受减瘤手术的mRCC患者,单用靶向药物治疗疗效非劣于减瘤术后序贯使用靶向药物。因此,对于mRCC患者,根据患者具体的情况制定个性化的治疗方案显得尤为重要。
⒉系统治疗
(1)临床试验
NCCN推荐参加临床试验仍是晚期肾癌的患者的优先选项。
⑵透明细胞为主型肾癌的系统治疗(表14)
1)透明细胞为主型肾癌的一线治疗
透明细胞型肾细胞癌的一线治疗首选分子靶向治疗。研究发现大部分肾透明细胞癌中细胞存在VHL基因缺失或失活,从而引起HIF基因上调,导致PDGF、VEGF、CaIX等基因过度表达,这些肿瘤发生、发展的生物学机制有可能是透明细胞型肾细胞癌分子靶向治疗的应用基础。
①舒尼替尼
舒尼替尼(sunitinib)是多靶点受体酪氨酸激酶抑制剂,主要作用靶点为血管内皮生长因子受体1-2(VEGFR1-2)、血小板衍生生长因子受体(PDGFR-α,PDGFR-β)、干细胞生长因子受体(c-KIT)以及FMS样酪氨酸激酶3(FLT-3),具有抗肿瘤血管生成、抑制肿瘤细胞增殖的作用。
2007年新英格兰杂志报道舒尼替尼与α干扰素1:1对比一线治疗转移性肾透明细胞癌Ⅲ期临床研究,共入组750例患者,90%患者为MSKCC中低度风险,中位PFS分别为11个月和5个月(HR 0.42,95% CI 0.32~0.54;P<0.001),客观缓解率分别为31%和6%(P<0.001),中位生存期分别为26.4个月和21.8个月(P=0.051)。从而奠定了舒尼替尼一线治疗肾透明细胞癌的地位。舒尼替尼一线治疗中国转移性肾细胞癌患者的多中心Ⅳ期临床研究结果显示客观有效率为31.1%,其中位PFS为14.2个月,中位OS为30.7个月。
基于上述临床数据,推荐舒尼替尼用于晚期透明细胞型肾细胞癌的一线治疗,用法为:50mg,qd 口服,4/2方案(服药4周,停药2周)给药。考虑舒尼替尼4/2给药方案血液学毒性不良反应发生率高,可选择2/1方案(服药2周,停药1周),耐受性提高,疗效未受影响。
②索拉非尼
索拉非尼(sorafenib)是最早上市用于转移性肾癌的多靶点受体酪氨酸酶抑制剂,具有双重抗肿瘤作用:一方面通过抑制RAF/MEK/ERK信号传导通路,另一方面作用于VEGFR、PDGFR,以及c-KIT、FLT-3、MET等靶点,抑制肿瘤生长。
2009年临床肿瘤学杂志报道索拉非尼与α干扰素1∶1对比一线治疗转移性肾透明细胞癌Ⅱ期临床研究,共入组189例患者,索拉非尼 400mg 每天2次,α干扰素900万单位每周3次,索拉非尼组进展后可以加量至600mg 每天2次,干扰素组进展后可以交叉到索拉非尼组。索拉非尼与α干扰素中位PFS分别为5.7个月和5.6个月,两组出现肿瘤缩小的比例分别为68.2%和39.0%,索拉非尼组有着更好的生活质量评分,耐受性更好。后续一项将索拉非尼作为对照用于转移性肾癌一线治疗的国际多中心Ⅲ期临床试验(TIVO-1研究)显示索拉非尼客观有效率为24%,中位PFS时间为9.1个月,中位总生存时间为29.3个月。国内索拉非尼的注册临床研究为一项来自研究者发起的多中心临床研究(IIT研究),共纳入62例患者,结果显示客观有效率为19.4%,疾病控制率为77.4%,中位PFS为9.6个月。由于索拉非尼一线治疗缺乏有效的大型研究结果且替代药物越来越多,目前NCCN指南不推荐索拉非尼一线治疗肾透明细胞癌。
近年一项国内多中心研究对845例晚期肾癌患者一线索拉非尼或舒尼替尼治疗后的生存和预后因素进行了回顾性分析,结果显示索拉非尼组与舒尼替尼组的中位PFS时间分别为11.1个月和10.0个月(P = 0.028),两组的中位OS无差异,均为24个月。由于索拉非尼具有良好的耐受性及在亚洲人群显示了较高的有效率,因此目前在国内索拉非尼仍在部分肾癌患者推荐为一线治疗方案。
③培唑帕尼
培唑帕尼(pazopanib)是多靶点受体酪氨酸激酶抑制剂,其主要作用靶点为VEGFR1~3、PDGFRα-β和c-KIT。
培唑帕尼治疗转移性肾癌的临床数据来源于其国际多中心Ⅲ期临床研究,结果显示培唑帕尼的中位PFS为11.1个月,客观缓解率为30%,显著优于安慰剂对照组,最终生存分析显示中位OS为22.6个月。另外一项培唑帕尼与舒尼替尼对照用于转移性肾癌一线治疗的国际多中心Ⅲ期临床研究(COMPARZ研究),国内多家中心参与了该临床试验,独立评估显示培唑帕尼与舒尼替尼的中位PFS分别为8.4与9.5个月,统计学达到非劣效,次要研究终点方面:ORR分别为31%与25%,中位OS分别为28.4与29.3个月,生活质量评分培唑帕尼优于舒尼替尼。该研究共纳入包含中国受试者在内共计367例的亚洲患者,亚组分析显示亚洲患者培唑帕尼治疗组中位无进展生存时间为8.4个月,与欧美人群无显著性差异。
基于上述临床数据,推荐培唑帕尼用于晚期透明细胞型肾细胞癌的一线治疗,用法为800mg,qd。
④阿昔替尼
阿昔替尼(axitinib)为新一代VEGFR1~3的受体多靶点酪氨酸激酶抑制剂。2013年柳叶刀杂志报道随机对照Ⅲ期临床研究,288例患者按照阿昔替尼与索拉非尼2∶1入组一线治疗晚期肾透明细胞癌,中位PFS分别为10.1个月和6.5个月(HR 0.77,95% CI 0.56~1.05)。尽管PFS延长了3.6个月,由于入组例数偏少,统计学无显著差异,但仍表现出阿昔替尼一线治疗肾透明细胞癌的有效性。基于临床研究数据,推荐阿昔替尼可以作为晚期肾透明细胞癌患者的一线治疗,具体用法为5mg,bid。
⑤卡博替尼
卡博替尼(cabozantinib)是针对VEGFR、MET、AXL等靶点的口服小分子激酶抑制剂,一项Ⅱ期多中心随机研究(CABOSUN)比较了卡博替尼和舒尼替尼一线治疗中危或高危(Heng评分)肾透明细胞癌患者的疗效。157例患者按照1∶1的比例随机接受一线卡博替尼(60mg,qd)或者舒尼替尼(50mg,4/2方案)治疗,结果显示卡博替尼组PFS显著优于舒尼替尼治疗组,两组中位PFS分别为8.2与5.6个月(P = 0.012),ORR分别为46%和18%,OS分别为30.3与21.8个月。
基于国外临床研究数据,推荐卡博替尼可以作为中高危晚期肾透明细胞癌患者的一线治疗,具体用法为60mg,qd。
⑥贝伐珠单抗联合干扰素
贝伐珠单抗(bevacizumab)为抗血管生成的抗VEGF单克隆抗体,其与IFN-α联合用于转移性肾癌的一线治疗,其主要的Ⅲ期临床数据来自国外的AVOREN研究以及CALGB90206研究,均证实了其临床疗效。AVOREN研究结果显示贝伐珠单抗联合干扰素-α一线治疗获得的中位PFS为10.2个月、客观有效率为30.6%,中位OS达到23.3个月,均优于单纯干扰素对照组。另一项大宗临床试验CALGB 90206研究也获得了类似的结果。国内贝伐珠单抗的适应证是用于转移性结直肠癌的治疗,尚缺乏治疗转移性肾癌的相关临床数据。
基于上述临床数据,推荐贝伐珠单抗联合IFN-α可以用于晚期透明细胞型肾细胞癌的一线治疗,具体用法为:贝伐珠单抗 10mg/kg,q2w,IFN-α 9MIU,tiw。
⑦替西罗莫司
替西罗莫司(temsirolimus,CCI-779)为mTOR抑制剂,除了通过抑制mTOR 信号抗肿瘤作用,还具有抑制血管生成作用,主要抑制缺氧诱导因子HIF-1的转录,减少对血管相关生长因子如VEGF/PDGF/TGF等的刺激,从而达到抑制肿瘤血管生成的作用。
替西罗莫司一线治疗转移性肾癌的Ⅲ期临床数据来自国际多中心随机对照Ⅲ期临床研究(ARCC研究),入组患者均为预后评分为高危的患者,结果显示替西罗莫司单药治疗的中位OS为10.9个月,中位PFS为5.5个月,明显优于IFN-α治疗组。一项替西罗莫司治疗亚洲人群非随机单臂开放性Ⅱ期临床研究,入组了中国、日本及韩国82例转移性肾癌患者,结果显示临床获益率为48%,客观有效率为11%,中位PFS时间为7.3个月。
替西罗莫司未在中国批准上市,但基于上述临床数据,推荐替西罗莫司可以用于晚期透明细胞型肾细胞癌高危患者的一线治疗,用法为:25mg,qw。
⑧免疫治疗
纳武单抗(Nivolumab)是一种结合于程序性死亡受体-1(PD-1)的单克隆抗体。伊匹单抗(Ipilimumab)是一种人类的细胞毒性T淋巴细胞抗原4(CTLA-4)的阻断抗体。CheckMate214研究是一项多中心随机对照Ⅲ期临床研究,评估纳武单抗联合伊匹单抗对比舒尼替尼一线治疗晚期/转移性中高危肾癌(1082例)的效果。结果显示在IMDC中高危晚期肾癌的一线治疗中,联合治疗组与舒尼替尼组在客观缓解率(42%对27%,P<0.001)及中位总生存期(未达到对26个月,P<0.001)方面均有明显获益,且耐受性良好。基于此研究结果,2018年4月FDA批准纳武单抗联合伊匹单抗作为IMDC中高危晚期肾癌的标准一线治疗。
⑨细胞因子治疗
细胞因子治疗多集中于早年的研究,主要为IFN-α和IL-2。2002年JCO杂志报道经IFN-α治疗的463例晚期肾细胞癌患者的回顾性分析,中位生存期13个月,中位TTP为4.7个月,其中高危、中危和低危患者生存期分别为5个月、14个月和30个月。2003年cancer杂志报道了173例转移性肾细胞癌患者经IL-2为基础治疗的回顾性分析,中位生存期13个月,1年、3年和5年生存率分别为92%、61%和41%。目前细胞因子一般不作为一线首选治疗。
结合我国具体情况,认为对于不能接受靶向药物治疗的转移性肾透明细胞癌患者,可以推荐细胞因子治疗作为替代治疗,其中大剂量IL-2可以用于一般情况较好,心肺功能正常的转移性肾透明细胞患者治疗,用法为:18 MIU/d,IH,5d/w×1w,9MIU q12h d1-2,9MIU qd d3-5×3w,休1周后重复。但高剂量IL-2治疗,严重不良反应发生率高,需严密监测。IFN-α的用法为:每次9MIU,IH,3次/周,共12周。
2)透明细胞为主型肾癌的后续治疗
①阿昔替尼
2011年柳叶刀杂志报道随机对照Ⅲ期临床研究(AXIS研究),针对一线治疗失败(绝大部分为细胞因子或舒尼替尼)的晚期肾细胞癌二线治疗,共723例患者按照1:1分别接受阿昔替尼和索拉非尼治疗,中位PFS分别为6.7个月和4.7个月(HR 0.665;95% CI 0.544~0.812;P<0.0001),有效率分别为19%和9%(P=0.0001),一线为细胞因子治疗的中位PFS分别为12.1个月和6.5个月(P<0.0001),一线为舒尼替尼的中位PFS分别为4.8个月和3.4个月(P=0.01),中位生存期分别为20.1个月和19.3个月。一项亚洲转移性肾癌患者二线接受阿昔替尼治疗的注册临床研究,其中大部分为中国患者,结果显示阿昔替尼中位PFS为6.5个月,客观有效率为23.7%。亚组分析显示既往接受舒尼替尼治疗患者二线接受阿昔替尼的中位PFS时间为4.7个月。基于上述临床试验结果,推荐阿昔替尼作为转移性肾癌的二线治疗,具体用法为阿昔替尼 5mg,bid。
②依维莫司
依维莫司(everolimus)为口服给药的mTOR抑制剂,其用于转移性肾癌的临床数据主要来自于2008年柳叶刀杂志报道的一项国际性多中心随机对照Ⅲ期临床研究(RECORD-1研究)。经舒尼替尼或索拉非尼治疗后进展的晚期肾细胞癌患者按照2∶1比例分别依维莫司和安慰剂治疗,最终统计中位PFS分别为4.9个月和1.9个月(HR 0.33;P <0.001),安慰剂组患者进展后有80%交叉到依维莫司组,故两组中位生存期无明显差异,分别为14.8个月和14.4个月。依维莫司常见的不良反应为胃炎、皮疹和乏力。一项国内患者接受依维莫司治疗的多中心注册临床研究(L2101研究),证实了依维莫司作为TKI治疗失败后二线靶向治疗的疗效及安全性,疾病控制率61%,中位PFS为6.9个月,临床获益率为66%,1年生存率为56%,1年无进展生存率为36%。
基于上述临床试验结果,推荐依维莫司作为转移性肾癌TKI治疗失败后的二线治疗药物,具体用法为依维莫司 10mg,qd。
③索拉非尼
2009年临床肿瘤学杂志报道Ⅲ期随机对照临床研究,针对一线治疗失败(绝大部分为细胞因子)的晚期肾透明细胞癌患者,一线治疗至少持续8个月,ECOG 0~1分,共903例患者分别接受索拉非尼和安慰剂治疗,两组的PFS分别为5.5个月和2.8个月,中位生存期分别为17.8个月和14.3个月(HR = 0.78;P =0.029)。
④舒尼替尼
舒尼替尼针二线治疗经细胞因子治疗后进展的转移性肾细胞癌患者同样表现出一定有效性。2006年JCO杂志报道回顾性研究,63例经细胞因子治疗后进展的肾细胞癌患者二线接受舒尼替尼治疗,有效率达40%,中位PFS为8.7个月。同样,2006年JAMA杂志报道106例患者的回顾性研究,有效率34%,中位PFS为8.3个月。
⑤卡博替尼
卡博替尼二线治疗晚期肾透明细胞癌与依维莫司比较有明显的生存优势,2016年Lancet Oncol报道METEOR研究最终结果,针对一线接受VEGFR-TKI治疗后进展的肾透明细胞癌患者,1∶1接受卡博替尼与依维莫司治疗,中位生存期分别为21.4个月和16.5个月(HR 0.66,95% CI 0.53~0.83;P=0.00026),同样PFS明显提升,有效率分别为17%和3%。
卡博替尼尚未在中国批准上市,但基于上述国外临床试验结果,推荐卡博替尼作为转移性肾癌TKI治疗失败后的二线治疗药物,具体用法为卡博替尼 60mg,qd。
⑥纳武单抗
2015年CheckMate 025研究结果显示针对接受过1-2种治疗后进展的肾透明细胞癌患者,按照1∶1接受纳武单抗和依维莫司治疗,中位生存期分别为25.0个月和19.6个月,有效率分别为25%和5%,中位PFS分别为4.6个月和4.4个月。3/4度不良反应发生率分别为19%和37%。
⑦仑伐替尼+依维莫司
仑伐替尼(lenvatinib)为一新型受体酪氨酸激酶抑制剂,主要靶点为VEGFR1-3、成纤维细胞生长因子受体1~4(FGFR1~4)、PDGFR-α、RET以及KIT。2016年Lancet Onco报道仑伐替尼联合依维莫司二线治疗肾透明细胞癌的Ⅱ期临床研究结果,153例患者随机接受仑伐替尼联合依维莫司治疗、仑伐替尼单药治疗和依维莫司单药治疗,联合组与依维莫司组中位PFS分别为14.6个月和5.5个月,中位生存期分别为25.5个月和15.4个月,仑伐替尼单药组中位生存期18.4个月。
⑧培唑帕尼
培唑帕尼一线治疗的Ⅲ期试验中有202例患者为细胞因子治疗后进展的患者,培唑帕尼与安慰剂的中位PFS分别为7.4个月和4.2个月。另一项56例患者的Ⅱ期研究显示,针对舒尼替尼或贝伐珠单抗治疗后失败患者,培唑帕尼治疗有效率27%,中位PFS为7.5个月,2年生存率43%。
⑨替西罗莫司
替西罗莫司作为舒尼替尼治疗失败的肾细胞癌患者的二线治疗,中位PFS为4.28个月,中位生存期12.27个月。
3)靶向药物的贯序应用
2006年8月至2011年6月意大利回顾性研究,收集mRCC患者接受三线靶向治疗的数据,旨在比较2种治疗顺序:VEGFi–VEGFi–mTORi vs. VEGFi–mTORi–VEGFi. 其中临床上最常用的3种方案为:舒尼替尼-索拉非尼-依维莫司(SuSoEv)、索拉非尼-舒尼替尼-依维莫司(SoSuEv)、舒尼替尼-依维莫司-索拉非尼(SuEvSo)。TKI-TKI-mTOR与TKI-mTOR-TKI比较,中位PFS分别为36.5个月和29.3个月(P=0.059),中位生存期分别为50.7个月和37.8个月(P=0.004),从而提示TKI-TKI-mTOR的治疗顺序可能更加合理。
4)靶向药物的联合应用
2016年Lancet Onco报道仑伐替尼联合依维莫司二线治疗肾透明细胞癌的Ⅱ期临床研究结果,153例患者随机接受仑伐替尼联合依维莫司治疗、仑伐替尼单药治疗和依维莫司单药治疗,联合组与依维莫司组中位PFS分别为14.6个月和5.5个月,中位生存期分别为25.5个月和15.4个月,仑伐替尼单药组中位生存期18.4个月。
5)靶向药物与免疫制剂的联合应用
2017年ESMO会议报道,仑伐替尼联合pembrolizumab治疗肾细胞癌的Ⅱ期研究结果,一线治疗组有效率高达83%(10/12),二线以上治疗组有效率也达到50%(9/18)。

⑶非透明细胞型肾癌的系统治疗
晚期非透明细胞癌患者由于样本量少,缺乏相应的大宗随机对照临床试验。舒尼替尼、索拉非尼以及依维莫司的扩大临床研究以及小样本的Ⅱ期研究显示这些靶向药物治疗非透明细胞型肾癌有效,但其疗效要差于透明细胞型肾癌(表15)。

1)舒尼替尼
对于非透明细胞型肾细胞癌的研究目前多为Ⅱ期临床研究,一项涉及31例患者的研究中,对于非透明细胞癌舒尼替尼的有效率为36%,中位PFS为6.4个月;另一项包括53例患者的研究中,舒尼替尼/索拉非尼的有效率为23%,中位PFS为10.6个月。
ASPEN研究中,108例非透明细胞癌初治患者随机接受舒尼替尼和依维莫司治疗,中位PFS分别为8.3个月和5.6个月,低危和中危组中位PFS分别为14.0个月与5.7个月、6.5个月与4.9个月;在高危组中依维莫司略占优势,但无统计学意义(4.0个月与6.1个月)。
ESPN研究中,68例患者随机接受舒尼替尼和依维莫司治疗,一线治疗中,两组中位PFS分别为6.1个月和4.1个月(P=0.6),中位生存期分别为16.2个月和14.9个月(P=0.18)。
2)阿昔替尼
目前阿昔替尼针对非透明细胞肾细胞癌患者的治疗疗效和安全性并不明确,相关研究正在进行中。
3)索拉非尼
一项回顾性Ⅱ期临床研究显示,53例非透明细胞肾细胞癌患者接受舒尼替尼或索拉非尼治疗,有效率10%,中位PFS为8.6个月,中位生存期19.6个月。
4)贝伐珠单抗
一项Ⅱ期临床研究显示,41例肾乳头状癌患者接受贝伐珠单抗+厄罗替尼治疗,其中19例患者至少接受过一次系统治疗,HLRCC有效率60%,散发乳头状癌有效率29%,中位PFS分别为24.2个月和7.4个月。
另一项Ⅱ期临床研究显示,34例初治的非透明细胞癌患者接受贝伐珠单抗+依维莫司治疗,中位PFS和OS分别为11.0个月和18.5个月,有效率29%。
5)卡博替尼
目前卡博替尼针对非透明细胞肾细胞癌患者的治疗疗效和安全性并不明确,相关研究正在进行中。
6)厄洛替尼
一项Ⅱ期临床研究显示,41例肾乳头状癌患者接受贝伐珠单抗+厄罗替尼治疗,其中19例患者至少接受过一次系统治疗,HLRCC有效率60%,散发乳头状癌有效率29%,中位PFS分别为24.2个月和7.4个月。
7)依维莫司
一项Ⅱ期临床研究显示,34例初治的非透明细胞癌患者接受贝伐珠单抗+依维莫司治疗,中位PFS和OS分别为11.0个月和18.5个月,有效率29%。
8)仑伐替尼+依维莫司
目前仑伐替尼+依维莫司针对非透明细胞肾细胞癌患者的治疗疗效和安全性并不明确,相关研究正在进行中。
9)纳武单抗
目前纳武单抗针对非透明细胞肾细胞癌患者的治疗疗效和安全性并不明确,相关研究正在进行中。
10)培唑帕尼
一项意大利的回顾性研究,37例非透明细胞性肾细胞癌患者一线接受培唑帕尼治疗,疾病控制率81%,有效率27%,中位PFS和OS分别为15.9个月和17.3个月。
11)替西罗莫司
一项回顾性的ARCC试验显示替西罗莫司治疗非透明细胞癌,中位生存期11.6个月,针对MSKCC评分高危组替西罗莫司为Ⅰ类推荐。
12)化疗
2018年NCCN肾癌指南推荐在肉瘤样和快速进展的肾细胞癌肿使用吉西他滨和多柔比星的联合方案可能是一种选择,具体为多柔比星(50 mg/m2)和吉西他滨(1500或2000 mg/m2)30分钟,每 2~3周1次,给与粒细胞集落刺激因子支持治疗。
⒊姑息性放疗
对局部瘤床复发、区域或远处淋巴结转移、骨骼或肺转移患者,姑息放疗可达到缓解疼痛、改善生存质量的目的。
⒋特殊部位转移的治疗原则
肾癌常见的转移部位分别为肺(45.2%)、骨(29.5%)、淋巴结(21.8%)、肝(20.3%)、肾上腺(8.9%)、脑(8.1%)、腹膜后(6.9%)等。其中肝、骨、脑的转移由于具有压迫周围神经或组织、严重影响生活质量以及预后不良等特点而在处理上存在一些特殊性。
(1)肾癌骨转移
肾癌骨转移部位多见于脊柱、骨盆和四肢近端骨骼,主要症状为病变部位进行性疼痛加重;在X线摄片下主要表现为溶骨性骨质破坏,因此转移部位容易发生病理性骨折,甚至压迫脊髓引起截瘫。此类患者应采用以靶向药物为主,结合手术、放疗、骨保护剂等相结合的综合治疗。
椎体是常见的肾癌骨转移部位,根据脊柱转移瘤NOMS(Neurologic,Oncologic,Mechanical and Systemic)治疗规范,对于包括肾癌在内的常规放疗不敏感的椎体转移瘤,推荐SBRT或者手术联合SBRT的治疗模式。文献报道,SBRT治疗肾癌椎体转移瘤,1年局控率高达71%∼90%,1年疼痛控制率高达82%,3度或以上严重不良反应发生概率仅0%∼2%。
对孤立或承重骨转移灶可考虑手术方法切除转移灶;承重骨骨转移伴有骨折风险的患者可采用预防性内固定术等方法以避免骨相关事件的发生。对于已出现病理性骨折或脊髓的压迫症状符合下列3个条件的患者推荐首选手术治疗:①预计患者存活期>3个月;②体能状态良好;③术后能改善患者的生活质量,有助于接受进一步的靶向治疗、放疗和护理。经皮椎体成形术可用于治疗脊柱溶骨性破坏和椎体病理性塌陷,可提高转移部位硬度和受力压强,缓解局部疼痛。局部姑息性低剂量放射治疗对减轻骨转移疼痛有一定作用。另外,同时使用骨保护剂药物,包括双膦酸盐和地诺单抗、镭-223,可减少骨相关事件的发生。
2016年ASCO年会的一项METEOR研究的亚组分析显示,METEOR研究纳入的658例晚期肾癌患者中,有142例患者存在骨转移,其中的112例患者同时存在骨和内脏转移。结果显示,骨转移患者接受卡博替尼治疗后的中位PFS是7.4个月,而依维莫司组为2.7个月;而对于同时存在骨和内脏转移的患者,卡博替尼或依维莫司治疗后的中位PFS分别为5.6个月和1.9个月,提示卡博替尼可能适合用于肾癌骨转移患者的治疗。
(2)肾癌脑转移
对脑转移灶,放疗的效果优于外科手术治疗,且放疗可以兼顾多发脑转移,配合地塞米松和脱水剂可以明显缩小肿瘤及水肿带,缓解颅内高压症状和其他神经症状。对体能状态良好、单纯脑转移的患者(脑转移灶≤3个,脑转移瘤最大直径≤3cm)首选立体定向放疗(γ刀、X刀、三维适形放疗、调强适形放疗)或脑外科手术联合放疗;对多发脑转移患者(脑转移灶>3个,脑转移瘤最大直径>3cm),可考虑行全颅放疗。然后需根据患者的耐受力,进行全身抗肿瘤药物治疗。
(3)肾癌肝转移
肾癌肝转移患者,通常预后较差,应首先考虑全身靶向药物治疗,如全身治疗无效,可考虑联合肝脏转移灶的局部治疗,如消融治疗、经肝动脉化学栓塞术(TACE)、立体定向放射治疗、以及高强度聚焦超声治疗(HIFU)等,可作为综合治疗的一部分,提高肝转移灶的局部控制,单独使用治疗意义不大。
七、随访
常规随访内容包括:①病史询问。②体格检查。③实验室检查,包括尿常规、血常规、尿素氮、肌酐、肾小球滤过率、乳酸脱氢酶、肝功能、碱性磷酸酶和血清钙。如果有碱性磷酸酶异常升高或(和)有骨转移症状如骨痛,需要进行骨扫描检查。④胸部平扫CT扫描。⑤肾肿瘤伴有急性神经系统迹象或症状的患者须即刻进行头部神经系统横断面CT或MRI扫描或基于相应节段症候的脊髓扫描。
(一)术后随访
对接受手术治疗的pT1N0/NxM0期肾癌患者应在术后3~12个月内做腹部CT或MRI检查作为基线片,以后每年进行1次,连续3年进行腹部影像学超声、CT或MRI检查,每年1次连续3年行胸部CT以确定是否有肺转移。对接受手术治疗的pT2~4N0/NxM0肾癌患者影像学检查时限改为每6个月1次至少持续3年,此后,每年1次。
(二)局部治疗患者的随访
对接受冷冻和射频等局部治疗的pT1aN0/NxM0期肾癌患者,应在术后3~6个月内做腹部CT或MRI检查作为基线片,以后每年进行1次(包括腹部和胸部影像学检查);如果随访中发现原肾脏病灶增大、出现新的强化、或出现新病灶,则需要对病灶进行穿刺活检。
(三)晚期患者的随访
对接受全身系统治疗的复发/转移性Ⅳ期肾癌患者,应尽可能在系统治疗前对全身所有可评价病灶(病灶最大径超过1cm)进行CT或MRI的影像学检查,作为基线片,以后应根据病情和治疗方案需要,每6~16周进行相同的影像学检查比较病灶大小、数量的变化以评价系统治疗的疗效。
