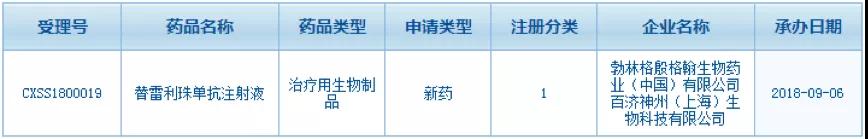
医药网11月14日讯 11月13日,界面新闻报道称,国家药监局药品审评中心(CDE)已结束百济神州PD-1替雷利珠单抗注册申请的技术审评工作,品种技术审评建议结论为“批准生产”。换言之,距离百济神州PD-1替雷丽珠单抗的正式获批仅差临门一脚。
凑巧的是,当日百济神州也公布了2019年第三季度财务业绩:2019 年第三季度,ABRAXANE®、瑞复美及维达莎®在中国销售为企业带来的产品收入总计5014万美元——这也是百济神州同期收入的总数;而同期的净亏损则达到3.0736亿美元。相较之下,2018年同期的净亏损为1.4403亿美元。
即将获批的替雷丽珠单抗可以让百济神州摆脱成立9年尚未推出一款自研新药、营收依赖于从其他药企所引进药品的窘况,然而作为国内第6款获批的PD-1、第4个获批的国产PD-1产品能否让企业摆脱连年亏损状态,恐怕还是个疑问。
PD-1竞争激烈 但尚有空间
目前已推进至第三天的国家医保谈判中,已上市的PD-1品种正展开贴身肉搏,其中可能有2~3家产品能凭降价进入医保报销系统。百济神州的替雷利珠单抗在此时拿到注册批件,国内PD-1市场格局调整无疑又将增加新的变数。
当然,依据相关规定,此次医保药品目录调入的西药和中成药是2018年12月31日(含)以前经国家药监局注册上市的药品。从时间节点看,包括今年5月获批的恒瑞PD-1也难纳入本次医保目录调整队列中。但无疑,医保的介入将大几率让PD-1药品的市场价格下调。
市场分析人士指出,结合中国每年新生
肿瘤病患将近400万,以及PD-1治疗临床常有喜人数据披露来看,已在国内上市的默沙东帕博利珠单抗、百时美施贵宝纳武利尤单抗、君实生物特瑞普利单抗、信达生物信迪利单抗和恒瑞
医药卡瑞利珠单抗5个产品竞争虽激烈,但仍有不少机会可发掘。天风证券也预计,到2020年国内抗肿瘤药市场将突破3000亿美元大关,市场空间巨大。
目前各上市PD-1药品在中国市场的表现也基本符合行业预期:默沙东的K药上半年销售额达10亿元,百时美施贵宝的O药上半年业绩4.3亿元,君实的特瑞普利单抗和信达的信迪利单抗也均超3亿元大关。
市场机会有待观察
据了解,百济神州的替雷利珠单抗此次申报的适应症为治疗复发/难治型经典霍奇金淋巴瘤,目前替雷利珠单抗有11项是三期临床试验,覆盖国内高发的肺癌、肝癌、食管癌、胃癌等癌种。
百济神州方面表示,替雷利珠单抗的优势在于在最大程度上减少由其他免疫细胞带来的负面调节作用。按照
企业的预期,近期将要完成的还有替雷利珠单抗用于治疗二、三线肝细胞癌(HCC)患者的全球2期临床试验的初步结果与药品监管机构沟通,以及对比多西他赛用于治疗二线非小细胞肺癌(NSCLC)患者的3期临床试验全球部分的患者入组。明年也计划推动替雷利珠单抗用于治疗局部晚期或转移性尿路上皮癌(UC)患者的新适应症上市批准。
当然,这也导致百济神州研发费用高企。截至2019年9月30日的第三季度,该公司研发费用已达2.3697亿美元,较去年同期增长0.8938亿美元。百济神州方面解释,增加的主要原因在于正在开展和新启动的后期关键性临床试验费用的持续增加、注册申报准备,以及产品上市前活动和供应相关的生产成本。
不过,新入“战场”的PD-1产品,百济神州是否能够让自研
药品分得可观市场份额,仍未可知。此外,本月初安进以27亿美元购买百济神州股份扩大后所发行股本的20.5%,双方协议将共同承担研发费用合作开发药品。未来,拥有自研产品的百济神州如何平衡渠道也有待观察。