发布时间:2020年08月13日 08:55:18 来源:振东健康网
尹娜,郭震,付金凤,张磊,王梦茹,沈文荣,张晋
(江苏省肿瘤医院CT室,江苏南京210009)
【摘 要】目的:探讨肝脏肿瘤射频消融术后3.0TMRI及CT在消融病灶疗效评估与随访中的应用。方法:回顾性分析2017年12月至2018年6月本院收治的75例行射频消融术肝脏恶性肿瘤患者的临床及影像学资料。所有患者术后均行肝脏多层螺旋CT及3.0TMRI检查,根据改良实体瘤疗效评价标准(mRECIST),应用受试者工作特征曲线(ROC曲线)分析两种不同影像学检查对射频消融术后局部疗效评价的价值。结果:CT和3.0TMRI诊断肝脏肿瘤消融术后肿瘤局部疗效的ROC曲线下面积分别为0.733和0.917。CT图像评价肿瘤局部疗效的敏感度、特异度、准确度分别为86.7%、60%、81%,3.0TMRI的分别为93.3%、90%、96%。结论:3.0TMRI在评估行肿瘤射频消融术后局部疗效方面明显优于CT,能准确且及时地对病灶进行评估,对疾病的诊疗和预后有重要的临床意义。
【关键词】磁共振成像;体层摄影术,X线计算机;局部疗效;射频消融术;肝脏肿瘤
[中图分类号]R730.55;R735.7 [文献标识码]A [文章编号]1671-7562(2020)03-0311-06
Evaluation of local efficacy of ablation of liver tumor on 3.0 T MRI and CT
YIN Na,GUO Zhen,FU Jinfeng,ZHANG Lei,WANG Mengru, SHEN Wenrong,ZHANG Jin
(CT Room,Jiangsu Province Tumor Hospital,Nanjing 210009,China)
[Abstract] Objective:To explore the application of 3.0 T MRI and CT in the evaluation and follow-up of ablation focus of liver tumor after radiofrequency ablation.Methods:The clinical and imaging data of 75 patients with liver cancer treated by RFA from December 2017 to June 2018 were analyzed retrospectively.All patients underwent MSCT and MRI after operation.According to the mRECIST(modified Response Evaluation Criteria in Solid Tumors),ROC(Receiver Operating Characteristic)were used to analyze the value of two different imaging examinations for local efficacy after radiofrequency ablation.Results:The area under ROC curve of CT and MRI in the diagnosis of local curative effect of liver tumor after ablation was 0.733 and 0.917,respectively.The sensitivity, specificity and accuracy of CT images in evaluating the local curative effect of tumor were 86.7%,60% and 81%, while MRI images were 93.3%,90% and 96%,respectively.Conclusion:After radiofrequency ablation of liver cancer,MRI is superior to CT in evaluating the local effect of tumor,and can accurately and timely evaluate the focus,which has important clinical significance for the diagnosis and treatment of the disease and prognosis.
[Key words]magnetic resonance imaging;tomography,X-ray computed;local effect;ablation;liver tumor
射频消融作为微创消融术中最为成熟的治疗方式,现已广泛用于肝脏、肺部等实质性器官肿瘤的微创治疗中,国内外已有大量文献报道其对不可手术切除的肿瘤具有显著疗效。由于肿瘤形状的不规则[1],射频消融容易残留,这是射频消融治疗的不足之处,而早期发现残存病灶对行射频消融术尤为关键。射频消融术后影像学检查,如CT及MRI,是消融病灶的主要随访方式。
1、对象与方法
1.1研究对象
回顾性分析江苏省肿瘤医院2017年12月至2018年6月符合以下标准的患者:(1)经病理证实为原发或转移性恶性肝脏肿瘤;(2)病情不适合手术,并签署射频消融手术知情同意书;(3)于术后1~6个月内在本院行CT及MRI检查。影像图片排除标准:(1)因金属异物或运动产生伪影、设备伪影等;(2)分辨率低、对比度差、图像噪声等信噪比差。共75例患者(85个病灶)纳入研究,男46例,女29例;年龄26~71岁,平均(65.47±7.62)岁;其中肝脏肿瘤原发病灶34例(35个病灶),转移灶41例(50个病灶)。
1.2仪器
采用PHILIPSIngenia3.0T行磁共振检查。使用腹部相控阵线圈,进行常规序列扫描。(1)T1WI:TR3.7ms,TE1.32ms,层厚5mm,层间隔-2mm,FOV360mm×360mm、矩阵288×288,屏气采集;(2)T2WI(压脂方式为SPAIR):TR1200ms,TE83ms,矩阵288×288,FOV360mm×360mm,层厚5mm,层间距0.5mm,呼吸触发采集;(3)DWI(b=0、500、800s·mm-2):TR1730ms,TE73ms,层厚5mm,层间隔1mm,FOV360mm×360mm,矩阵288×288,呼吸触发采集;(4)增强扫描采用三维容积内插快速扰相行三期动态扫描,TR3.7ms,TE1.32ms,层厚5mm,层间隔-2mm,FOV360mm×360mm,矩阵288×288,屏气采集。高压注射器经肘部静脉注入对比剂(钆喷酸葡胺注射液,流速2ml·s-1、0.1mmol·kg-1)。采用GEDiscove750行CT扫描,扫描层厚5mm,螺距1.0。仰卧位进行平扫加三期动态增强扫描及延迟期扫描,造影剂为碘海醇,使用剂量是100ml,流速3ml·s-1。
1.3研究方法
1.3.1根据局部疗效肿瘤消融分类[2](1)完全消融:MRI显示病灶为短T1及短T2信号,弥散不受限,动态增强未见强化;CT显示病灶为低密度,肝脏三期均未见强化。(2)部分消融或肿瘤残留:MRI表现为病灶周围不规则增厚或结节,肿块边缘T1及T2信号稍长,DWI信号的增高及ADC值的降低;增强CT扫描病灶周围不规则强化,呈现快进快出征象。(3)局部肿瘤进展:完全消融病灶后期影像随访出现活性肿瘤。(4)新发肿瘤:术后影像发现消融区以外出现活性肿瘤。
1.3.2阅片判断由两名高年资的放射科医生采用双盲法阅片,若两者意见不同,经过商量最终获得诊断结论。MRI图像包括平扫及增强扫描图像、弥散加权成像(DWI)和ADC值图,CT图像包括平扫及增强扫描图片。将所有病灶的CT与MR图像采用4分制打分:1分,完全消融;2分,部分消融或肿瘤残留;3分,局部肿瘤进展;4分,新发肿瘤。
1.4统计学处理
采用SPSS18.0统计软件进行数据统计分析,运用受试者工作特征曲线(ROC曲线),以随访最终日期的影像学结果为金标准,根据曲线评价阅片者的诊断效能[3],分别计算CT与MRI评估的敏感度、特异度和准确度,以及ROC曲线下面积(AUC)。
2、结果
2.1术后情况
本组75例患者顺利完成射频手术治疗,术后常规止血,采用抗生素治疗5d。31例患者穿刺部位术后疼痛,给予止痛治疗1周后消失。15例患者出现发热症状,降温处理后好转。
2.2MRI及CT统计结果
在随访的85个消融病灶中,MRI检出完全消融病灶61个,部分消融24个(含局部肿瘤进展10个,新发肿瘤7个);CT检出完全消融58个,部分消融27个(含局部肿瘤进展11个,新发肿瘤5个)。阅片者对两者检查的评分结果见表1。计算MRI及CT检查两者AUC,分别为0.917和0.733,MRI的敏感度、特异度、准确度分别为93.3%、90%、96%,均高于CT的86.7%、60%、81%,差异具有统计学意义(P=0.033)。
2.3肝脏肿瘤消融后术不同疗效的MRI及CT检查结果
病例1:原发肝癌患者,肝右叶肿瘤消融术后1个月行MRI及CT检查(图1)。T2WI病灶周围炎性水肿期环形高亮信号(图1①A),T1WI显示消融区域中心呈等及低信号混杂信号(图1①B),常规T1WI及T2WI扫描未能判断是否消融完全。DWI可反映目标组织中水分子的热驱动运动,提供与肿瘤细胞性和细胞膜完整性相关的信息,测量ADC值可进行定量分析。完全消融病灶因为坏死的肿瘤细胞膜完整性破坏,膜通透性增加,水分子的扩散增加,表现DWI低信号,ADC图未见低信号改变(图1①C);增强后T1WI压脂(图1①D)及CT平扫增强(图1②)显示消融区域无强化,呈完全消融征象。
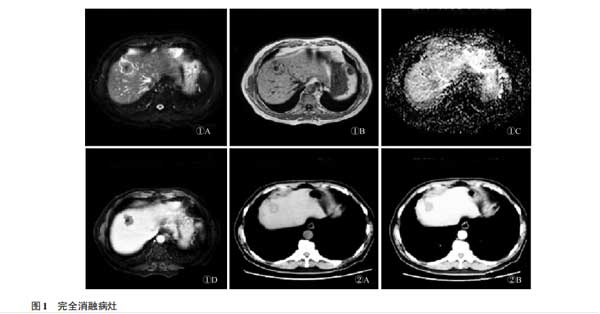
病例2:直肠癌肝脏多发转移患者。消融术后3个月复查,T2WI序列为稍高信号、增强序列强化及ADC值下降,DWI图可见结节状或片状高信号,表示该区域有弥散受限且原病灶范围扩大,灶周不均匀强化伴新发转移灶。见图2。
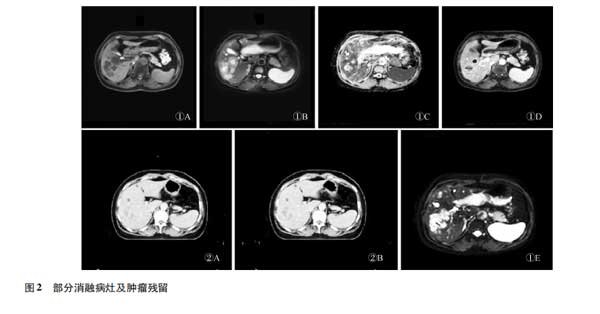
病例3:肝细胞癌患者。射频术后3个月复查。MRI显示肝左外叶边缘新发异常信号结节,T2WI压脂相显示高信号结节,T1WI低信号,DWI及ADC显示弥散受限,提示新发病灶;同期CT扫描却未见明显显影。见图3。本研究中MRI检出新发病灶7例,CT发现新发病灶5例,MRI先于CT检出远处转移灶2例。
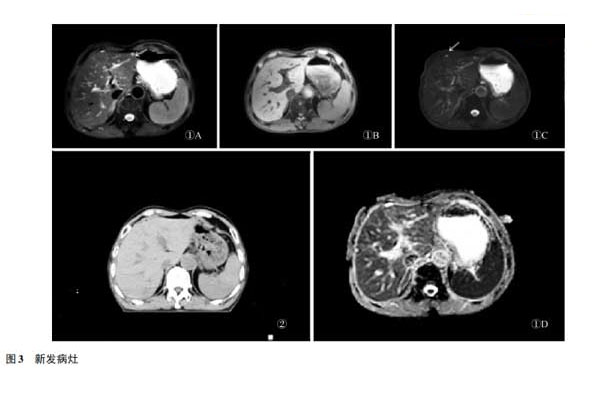
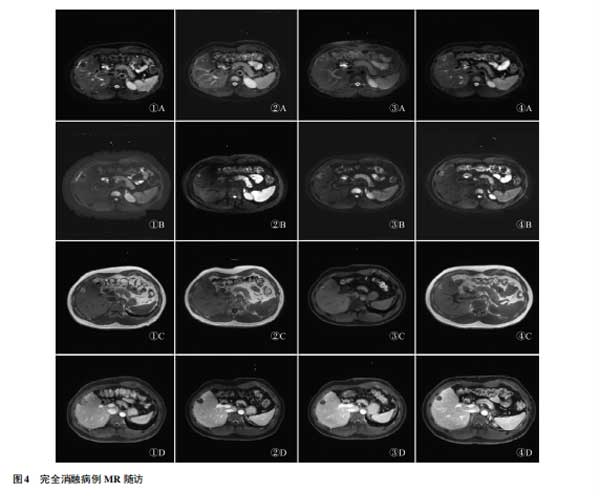
病例4:肝右叶原发性肝癌患者,图4①、②、③、④分别为消融术后1、3、6、12个月随访图像。术后1个月病灶T1WI呈完整环高信号(图4①C),弥散不受限,增强扫描未见异常对比强化,术后早期组织对热损伤的充血反应,病灶周围出现水肿带。T2WI出现环状高亮信号(图4①A)[4],可根据水肿环的连续性判断消融疗效的价值,在后期随访中逐渐消退(图4②~④),且病灶范围趋缩小,呈完全消融征象,消融效果良好。
3、讨论
目前,微创射频消融术对无手术指征的恶性肿瘤患者来说是首选的治疗方式,国内外多次报道其具有良好的疗效和安全性,是最为成熟的热损失治疗技术。射频消融对小肝癌治疗有较好的效果,小于3cm的小肝癌经过射频消融术后完全消融率达到93%[5]。初次消融完全是消融手术的关键,消融区能完全覆盖肿瘤病灶是手术成功的标志。在术后的随访中,选取优势影像检查及时了解局部疗效,较早地发现未消融病灶对患者来说具有至关重要的意义。
恶性肿瘤组织的MRI信号呈稍长T1和稍长T2,射频术后坏死病灶变为短T1和短T2信号。消融术后肿瘤病灶周围的组织会出现凝固性坏死,其病理改变分炎症期、纤维增生及恢复期3个阶段,这对术后随访的检查要求较高。部分病灶在[6]术后1个月炎症期内存在着蛋白的浓缩,会出现T1WI高信号,组织的脱水效应会呈现T2WI低信号、弥散受限的征象,可进行ADC值的测量以及动态增强扫描检查,通过时间-信号曲线来判断。本研究首次随访时间大多为术后1个月,消融肿瘤病灶在早期存在的炎症反应与存在残留的肿瘤也容易混淆,CT随访中假阳性与假阴性多于MRI,这与周围凝固灶的炎症充血反应有关。消融边缘血管细小,增强后强化不明显,CT无法明显显示病灶。MRI能清楚辨别病灶所在阶段:炎症反应阶段的病灶周围会出现逐渐强化的显影,在长期的随访中会逐渐减弱;增生阶段表现为其边缘为长T1、短T2信号,增强扫描不强化或表现为平衡期轻度强化,DW弥散加权(ADC值的测量)给所在阶段提供很大的支持。Yuan等[7]研究发现,ADC能准确鉴别肝癌坏死区域,特异度达100%,敏感度达92.3%,DWI的诊断效能有很重要的意义。完全消融病灶在CT增强图像上表现为低密度影且没有强化和没有快进快出的征象,在1个月左右随访中环绕消融病灶会出现高密度均匀较薄的强化带,在后期随访中会逐渐消失。CT观察肿瘤完全消融区可根据消融范围的体积不增大或进行性缩小来判断消融情况,且在多期增强扫描中未出现强化,但有文献报道[8]术后1年以上低密度区的消融范围周边仍可有病变的复发。本研究仅仅统计随访到1年内进行复查的患者,在以后的工作中有待延长随访时间,进一步探究CT检查对于恶性肿瘤射频术后疗效的评估价值。
首次随访完全消融的病灶在后期仍会出现活性肿瘤成分,肝脏消融肿瘤及远处复发有很多因素,包括血清AFP水平、血清DCP、术前肝功能Child-Pugh分级等;消融不完全也是其中很主要的原因,消融的范围有严格要求,消融边缘要超出病灶边缘5mm的区域,已达到防止肿瘤复发的作用,靠近动静脉、包膜的肿瘤病灶容易消融得不完全而易复发;影像随访的检查方式不同存在假阳性率,及早及时发现新发病灶对临床具有重要意义。MRI[9]在RFA术后对小病灶的显示更具有优势,在疗效评估和测量病灶大小方面比螺旋CT准确。吴海等[3]在1.5TMRI与CT对微波消融病灶进展情况进行研究,MRI在敏感度、特异度和准确度明显优于CT,本研究与其一致。通过MRI能及时观察病灶的坏死及复发,并且可实时观察病情进程情况,更直观地评价射频疗效。
MRI可多序列、多参数成像,具有高的软组织分辨力优势,且无辐射,无危害。3.0TMR在技术方面有很大提高,尤其MRI[10]在诊断肝细胞癌的灵敏度、特异度以及诊断的准确率方面有明显优势。MRI检查射频术后病灶、了解病灶情况,明显优于CT检查。多模磁共振成像技术具有丰富的诊断信息,能够更加准确定性术后消融疗效,辨别残留、复发的肝脏肿瘤组织,可为临床治疗提供有效的支持。
参考文献
[1]王东东,李晓光.肝癌射频消融后肿瘤残余的研究现状与进展[J].介入放射学杂志,2019,28(8):800-804.
[2]王广志,何新红.影像导引肝脏恶性肿瘤多模态消融治疗技术专家共识[J].介入放射学杂志,2018,27(7):603-607.
[3]吴海,陈延帆,许加峻,等.1.5TMR与多层螺旋CT在肝癌微波消融术后临床价值分析[J].医学影像学杂志,2016,26(11):2017-2019.
[4]宋吉慧,王丽娜,权力,等.肝脏恶性肿瘤射频消融术后早期FS-T2WI消融区周围水肿环评价消融疗效的应用[J].中国介入影像与治疗学,2019,16(6):328-332.
[5]曾鹏.经皮射频消融治疗小肝癌疗效及预后分析[D].长沙:中南大学,2014.
[6]高钦宗,王志伟,金征宇.肝癌热消融治疗后影像学评价的进展[J].医学研究杂志,2018,47(9):5-8.
[7]YUAN Z,LI W T,YE X D,et al.Utility of diffusion-weighted imaging to assess hepatocellular carcinoma viability following trans-arterial chemoembolization[J].Oncol Lett,2014,8(2):831-836.
[8]陈杰.MRI 引导下兔肝 VX2 肿瘤微波消融实验研究[D].福州:福建医科大学,2018.
[9]MULIER S,NI Y,JAMART J,et al.Localrecurenceafterhepatic radiofrequency coagulation:multivariate meta-analysis and review of contributing factors [J].Ann Surg,2005,242:158-171.
[10]张见增,胡海东,尤金涛,等.微小肝癌的 MRI 表现及诊断[J].临床放射学杂志,2017,36(11):1657-1661.
(现代医学2020,Mar;48(3):316-320)
